
将足量的CO2不断通入NaOH、Ba(OH)2、Na[Al(OH)4]的混合溶液中,生成沉淀与通入CO2的量的关系可表示为

A B C D
【答案】C
【解析】
试题分析:由于氢氧化铝是两性氢氧化物,能溶于氢氧化钠溶液中,而不能溶解在碳酸中。又因为碳酸的酸性强于氢氧化铝的,而HCO3-与AlO2-不能大量共存,所以将足量的CO2不断通入NaOH、Ba(OH)2、Na[Al(OH)4]的混合溶液中,发生反应的方程式依次为Ba(OH)2+2CO2=H2O+BaCO3↓、2NaOH+2CO2=Na2CO3+H2O、Na[Al(OH)4]+CO2=Na2CO3+2Al(OH)3↓+H2O、Na2CO3+H2O+CO2=2NaHCO3、BaCO3+H2O+CO2=Ba(HCO3)2,依次符合条件的曲线是选项C,答案选C。
考点:考查CO2与氢氧化钡、氢氧化钠以及偏铝酸钠混合液反应的有关判断


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
利用化学变化的递变规律,常可对某些物质的化学性质作出合理的推测,请判断下列各推测是否合理(填合理、不合理或不一定合理),并说明判断的理由。
(1)从红热的铜丝能在氯气中燃烧的事实,推测红热的铁丝也能在氯气中燃烧。
(2)从铁粉和硫粉加热条件下能发生反应的事实,推测铜粉和硫粉在相同加热条件下也一定能发生反应。
(3)从SO2通入Ba(OH)2溶液能产生白色沉淀的事实,推测SO2通入BaCl2溶液也能产生白色沉淀。
(4)从反应2CO2 +2Na2O2==2Na2CO3 +O2↑的事实,推测二氧化硫也一定能发生反应:
2SO2 +2Na2O2==2Na2SO3 +O2↑。
| 题号 | 是否合理 | 理 由 |
| (1) | ||
| (2) | ||
| (3) | ||
| (4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将右图所示实验装置的K闭合,
将右图所示实验装置的K闭合,
下列判断正确的是
A. 电极上发生还原反应
电极上发生还原反应
B.电子沿Zn a
a b
b Cu路径流动
Cu路径流动
C.片刻后甲池中c(SO42—)增大
D.片刻后可观察到滤纸b点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
研究人员最近发现了一种“水”电池,这种电池能利用淡水和海水之间含盐量的差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
A.Ag发生还原反应
B.正极反应式:5MnO2+2e- =Mn5O102-
C.每生成1mol AgCl转移2mol电子
D.Cl—不断 向“水”电池的正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化学基础(15分)
(1)含苯酚的工业废水必须处理达标后才能排放,苯酚含量在1 g·L-1 以上的工业废水应回收苯酚。某研究性学习小组设计下列流程,探究废水中苯酚的回收方法。
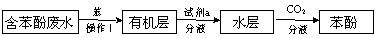
①可用 ▲ 为试剂检验水样中是否含有苯酚。
②操作I的名称为 ▲ ,试剂a的化学式为 ▲ 。
③通入CO2发生反应生成苯酚的化学方程式为 ▲ 。
(2)某有机物的分子式为C3H6O3。
①1 mol该有机物充分燃烧消耗的O2在标准状况下的体积为 ▲ L。
②若两分子该有机物能生成六元环状结构,写出该反应的化学方程式 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(实验题)50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。
回答下列问题: (1)从实验装置上看,图中尚缺少的一种玻璃仪器是_____________。
(2)烧杯间填满碎泡沫塑料的作用是_______________________________________。
(3)大烧杯上如不盖硬纸板,求得的中和反应的反应热的数值________(填“偏大” “偏小”或“无影响”)。
(4)实验中改用55 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和反应的反应热会________(填“偏大”“偏小”或“无影响”)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com