
下列微粒可以大量共存于同一溶液中的是( )
|
| A. | NH4+、CH3COO﹣、Ca2+、Cl﹣ | B. | Fe3+、Ag+、SO42﹣、NO3﹣ |
|
| C. | Cu2+、H+、S2﹣、NO3﹣ | D. | C6H5OH、Fe3+、K+、Cl﹣ |
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
下列有关物质用途的说法中,正确的是( )
A.玻璃容器可长期盛放各种酸 B.硝酸常用作金属铜加工前的酸洗
C.碳酸钠可用于治疗胃酸过多 D.三氧化二铁常用于生产红色油漆和涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是:
(CH3)2C O+HCN
O+HCN (CH3)2C(OH)CN
(CH3)2C(OH)CN
(CH3)2(OH)CN+CH3OH+H2SO4
CH2 C(CH3)COOCH3+NH4HSO4
C(CH3)COOCH3+NH4HSO4
90年代新法的反应是:
CH3C≡CH+CH3OH+CO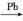 CH2
CH2 C(CH3)COOCH3
C(CH3)COOCH3
与旧法比较,新法的优点是(CD)
A. 原料无爆炸危险
B. 原料都是无毒物质
C. 没有副产物,原料利用率高
D. 对设备腐蚀较小
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产生活有密切的联系。以下说法正确的是
A.埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
B.气象环境报告中新增的“PM2.5”是对一种新分子的描述
C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
D.施肥时,草木灰(有效成分为K2CO3)与NH4Cl混合使用效果更好
查看答案和解析>>
科目:高中化学 来源: 题型:
三聚氰胺(化学式:C3N6H6)是一种重要有机化工原料。下图是我国科技工作者研制的以尿素为原料生产三聚氰胺的工艺——“常压气相一步法联产纯碱新技术”:
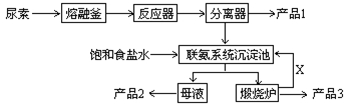
已知:以尿素为原料生产三聚氰胺的原理是:6 CO(NH2)2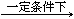 C3N6H6 +6 NH3+3CO2
C3N6H6 +6 NH3+3CO2
请回答:
(1)尿素的结构式为
(2)已知:产品1是本工艺的主产品,产品2是副产品,X为循环使用的物质,产品3为纯
碱。写出各主要成份的化学式:产品1 产品2 X
(3)联氨系统沉淀池中发生的化学反应方程式为:
(4)为了使母液中析出更多的产品2 ,常用的方法是
A、加入固体NaCl B、加入固体NaHCO3 C、通入CO2气体 D、通入NH3
(5)若生产过程中有4%的尿素损耗,每吨尿素理论上可得副产品纯碱 吨(精确到0.001)
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断正确的是( )
|
| A. | 原子半径由小到大的顺序:r(C)<r(D)<r(E) |
|
| B. | 元素D、E分别与A形成的化合物的热稳定性:E>D |
|
| C. | 元素D的最高价氧化物对应水化物的酸性比E的强 |
|
| D. | 元素B分别与A、C形成的化合物中化学键的类型不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
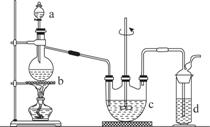
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂。它易溶于水,不溶于醇,受热、遇酸易分解。工业上可用反应:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2制得。实验室模拟该工业过程的装置如图所示。
回答下列问题:
(1)b中反应的离子方程式为________________,c中试剂为________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________。
(3)d中的试剂为________。
(4)实验中要控制SO2生成速率,可以采取的措施有___________________________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是______________________。
(6) 所得产品常含有少量Na2SO3和Na2SO4。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀盐酸、蒸馏水中选择)
①取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,________________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
②为减少装置C中生成Na2SO4的量,在实验过程中应注意的操作顺序是_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
运用有关概念判断下列叙述正确的是( )
A.1molH2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
C.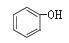 和
和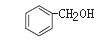 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
被称为“脑黄金”的DHA,是从深海鱼油中提取出的不饱和程度很高的脂肪酸,它的分子中有6个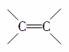 ,称为二十六碳六烯酸,则其甘油酯的分子结构简式为( )
,称为二十六碳六烯酸,则其甘油酯的分子结构简式为( )
A.(C25H51COO)3C3H5 B.(C25H39COO)3C3H5
C.(C26H41COO)3C3H5 D.(C26H47COO)3C3H5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com