
(8分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
(1)关于该反应的下列说法中,正确的是_______。
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0。
(2)该反应平衡常数K的表达式为_______________。
(3)温度降低,平衡常数K_____(填“增大”、“不变”或“减小”)。
(4)为探究反应原理,现进行如下实验:在体积为2L的密闭容器中,充入2mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如右图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2) 为:
________________________
(5)下列措施中能使n(CH3OH)/n(CO2)增大的有______。
A.升高温度; B.加入催化剂;
C.将H2O(g)从体系中分离; D.再充入1molCO2和3molH2;
E.充入He(g),使体系总压强增大。
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:2010年福建省季延中学高二下学期期末考试化学试题 题型:填空题
(8分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。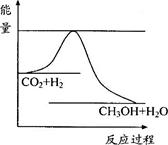
(1)关于该反应的下列说法中,正确的是_______。
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0。
(2)该反应平衡常数K的表达式为_______________。
(3)温度降低,平衡常数K_____(填“增大”、“不变”或“减小”)。
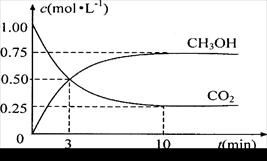
(4)为探究反应原理,现进行如下实验:在体积为2L的密闭容器中,充入2mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如右图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2) 为:
________________________
(5)下列措施中能使n(CH3OH)/n(CO2)增大的有______。
A.升高温度; B.加入催化剂;
C.将H2O(g)从体系中分离; D.再充入1molCO2和3molH2;
E.充入He(g),使体系总压强增大。
查看答案和解析>>
科目:高中化学 来源:2010年福建省高二下学期期末考试化学试题 题型:填空题
(8分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) 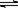 CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
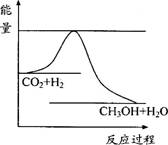
(1)关于该反应的下列说法中,正确的是_______。
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0。
(2)该反应平衡常数K的表达式为_______________。
(3)温度降低,平衡常数K_____(填“增大”、“不变”或“减小”)。
(4)为探究反应原理,现进行如下实验:在体积为2L的密闭容器中,充入2mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如右图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2) 为:
________________________

(5)下列措施中能使n(CH3OH)/n(CO2)增大的有______。
A.升高温度; B.加入催化剂;
C.将H2O(g)从体系中分离; D.再充入1molCO2和3molH2;
E.充入He(g),使体系总压强增大。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com