
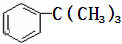 ②
②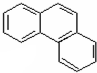 ③
③ ④
④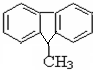 ⑤CH3CH=CHCH3.
⑤CH3CH=CHCH3.| A. | ②③ | B. | ①④ | C. | ①②④ | D. | ①⑤ |
分析 依据苯环、甲烷、乙烯的结构进行分析即可,甲基中C与四个H不可能共平面,据此H被甲基取代后,C原子不可能共平面.
解答 解:①丁基中间上的碳为四面体结构,所以碳原子不可能处于同一平面,故①选;
② 可以看作是相邻的两个苯环共用两个碳原子形成的,所以所有的碳原子都处在同一平面上,故②不选;
可以看作是相邻的两个苯环共用两个碳原子形成的,所以所有的碳原子都处在同一平面上,故②不选;
③ 苯为平面结构,该分子可以看成是两个甲苯中的甲基邻位碳原子与对位碳原子相连形成的,每个苯环上的碳原子(包括甲基碳)一定共面,这两个平面可以是一个平面,所以所有碳原子可能都处在同一平面上,故③不选;
苯为平面结构,该分子可以看成是两个甲苯中的甲基邻位碳原子与对位碳原子相连形成的,每个苯环上的碳原子(包括甲基碳)一定共面,这两个平面可以是一个平面,所以所有碳原子可能都处在同一平面上,故③不选;
④ 分子中含有两个苯环,每个苯环上的碳原子一定共面,但是甲基碳原子以及甲基相连的碳原子是烷烃的结构,一定不会共面,该分子中的所有碳原子不可能都处在同一平面上,故④选;
分子中含有两个苯环,每个苯环上的碳原子一定共面,但是甲基碳原子以及甲基相连的碳原子是烷烃的结构,一定不会共面,该分子中的所有碳原子不可能都处在同一平面上,故④选;
⑤CH3CH=CHCH3故,此为烯烃结构,乙烯中的六个原子均共平面,线两个甲基取代H的位置生成2-丁烯,四个碳原子可以共平面,故⑤不选;
故选B.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和甲醛的结构特点判断有机分子的空间结构.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
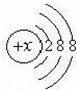 核外电子数相等的微观粒子不一定是同种微粒,今有几种微粒的核外电子层结构如图所示,请按要求填空:
核外电子数相等的微观粒子不一定是同种微粒,今有几种微粒的核外电子层结构如图所示,请按要求填空:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
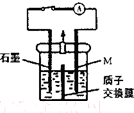 化学镀铜废液中含有一定量的CuS04,任意排放会污染环境,利用电化学原理可对废液进行回收处理,装置如图,其中质子交换膜只允许H+通过.
化学镀铜废液中含有一定量的CuS04,任意排放会污染环境,利用电化学原理可对废液进行回收处理,装置如图,其中质子交换膜只允许H+通过.| A. | 反应之前,应将含OH-的HCHO溶液加人到装置的左侧 | |
| B. | 右侧发生的电极反应式:HCH0-2e-+H20=HC0O-+3H+ | |
| C. | 若将质子交换膜换成阴离子交换膜,放电过程中,大量的OH-将向左侧迁移 | |
| D. | 放电一段时间后打开开关,移去质子交换膜,装置中可能会有红色固体、蓝色絮状物出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 只有①能和碳酸钠反应放出气体 | B. | ②和④互为同分异构体 | ||
| C. | ①②④都可以使溴水褪色 | D. | ④与H2加成后可以得到③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1mol丙烯中含碳原子数为3NA | |
| B. | 常温下,pH=13的NaOH溶液中含OH-数目为NA | |
| C. | 23gNa与足量氧气反应时转移的电子数为2NA | |
| D. | 标准状况下,22.4LCHCl3中含C-H键数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子或分子 | 要求 |
| A | Mg2+、SO42-、Cl-、NO3- | c(Mg2+)=c(SO42-) |
| B | Na+、Cu2+、I-、NH3•H2O | 在酸性高锰酸钾溶液中 |
| C | NH4+、Al3+、Cl-、NO3- | 滴加氨水有沉淀产生 |
| D | Cl-、Na+、Cr2O72-、C2H5OH | 溶液无色透明且遇甲基橙显红色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与浓氢溴酸卤代 | B. | 与浓硫酸共热消去 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com