
分析 反应3Cl2+8NH3=6NH4Cl+N2中,Cl元素化合价由0价降低到-1价,被还原,Cl2为氧化剂,N元素化合价由-3价升高到0价,被氧化,NH3为还原剂,结合元素化合价的变化和反应的方程式解答该题.
解答 解:(1)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为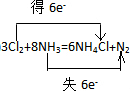 ,故答案为:
,故答案为: ;
;
(2)反应3Cl2+8NH3=6NH4Cl+N2中,Cl元素化合价由0价降低到-1价,被还原,Cl2为氧化剂,为还原产物NH4Cl,N元素化合价由-3价升高到0价,被氧化,NH3为还原剂,为氧化产物N2,
故答案为:Cl2;NH3;N2;NH4Cl;
(3)当有68g NH3参加反应时,n(NH3)=$\frac{68g}{17g/mol}$=4mol,其中有$\frac{1}{4}$的氨气被氧化,N元素化合价由-3价升高到0价,则转移电子的物质的量为4mol×$\frac{1}{4}$×3=3mol,
被氧化的氨气为4mol×$\frac{1}{4}$×17g/mol=17g;
故答案为:17.
点评 本题考查氧化还原反应,为高考高频考点,把握发生的化学反应及反应中元素的化合价变化为解答的关键,侧重基本概念和转移电子的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
| 盐酸 分子式: 相对分子量:36.5 密度:1.2g/ml HCI质量分数:36.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由反应①可知,Cl2是氧化剂,TiCl4是氧化产物 | |
| B. | 由反应①可知,可用CO在高温下把TiO2还原成Ti | |
| C. | 由反应②可知,若有24 g Mg参加反应,就可生成1 mol Ti | |
| D. | 由反应②可知,金属Mg的还原性比金属Ti的还原性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积相等,密度相等的CO和C2H4 | B. | 温度相同,体积相同的O2和N2 | ||
| C. | 质量相等,密度不等的N2和CO | D. | 压强相同、体积相同的N2和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不同的催化剂对化学反应速率的影响均相同 | |
| B. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| C. | 新法合成能在常温下进行是因为不需要锻炼化学键 | |
| D. | 新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展愿景 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 体积不变充入N2使压强增大 | B. | 体积不变充入O2使压强增大 | ||
| C. | 使体积增大到原来的2倍 | D. | 体积不变充入氦气使压强增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com