
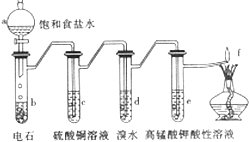
 如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )
如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )| A、制备乙炔的反应原理是:CaC2+2H2O→Ca(OH)2+C2H2↑ |
| B、c的作用是除去影响后续实验的杂质 |
| C、d中的有机产物与AgNO3溶液混合能产生沉淀 |
| D、e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、除去硫酸铜溶液中的硫酸亚铁以最终制备胆矾晶体:2Fe2++Cl2═2Fe3++2Cl- |
| B、Fe(OH)3与氢溴酸溶液混合:Fe(OH)3+3HBr═Fe3++3Br-+3H2O |
| C、用氨水吸收烟道气中的SO2:SO2+2NH3?H2O═2NH4++SO32-+H2O |
| D、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
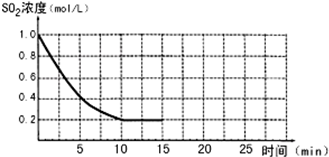 已知:2SO2(g)+O2(g)?2SO3(g);△H=-196kJ/mol,850K时,在2L固定容积的密闭容器中充入2mol SO2和2mol O2,10分钟后达到平衡,SO2浓度和时间关系如图.
已知:2SO2(g)+O2(g)?2SO3(g);△H=-196kJ/mol,850K时,在2L固定容积的密闭容器中充入2mol SO2和2mol O2,10分钟后达到平衡,SO2浓度和时间关系如图.查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
| A、若25<t1<t2,则a<1×10-14 |
| B、t2℃时,将一定物质的量浓度的盐酸与氢氧化钠溶液中和后,所得混合溶液pH=7,溶液呈中性 |
| C、25℃时,某Na2SO4溶液中c(SO42-)=5×10-4mol/L,取该溶液1 mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=1000:1 |
| D、t2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合,所得混合溶液的pH=2,则V1:V2=11:9(设混合后溶液的体积为原两溶液体积之和) |
查看答案和解析>>
科目:高中化学 来源: 题型:
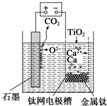 如图,石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质.图示装置工作时,生成的金属钙能还原二氧化钛制备金属钛.下列说法不正确的是( )
如图,石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质.图示装置工作时,生成的金属钙能还原二氧化钛制备金属钛.下列说法不正确的是( )| A、阳极反应式为C+2O2--4e-═CO2↑ |
| B、由TiO2制得1mol金属Ti,理论上外电路转移4mol电子 |
| C、制备金属钛前后,装置中CaO的量不变 |
| D、TiO2在阴极放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | ||
| Z | M | R |
| A、气态氢化物稳定性:X>Y |
| B、最高价氧化物的水化物的酸性:Y>M |
| C、R的氧化物的水化物是离子化合物 |
| D、Z、M、R的原子半径依次减小,最高化合价依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | ||||
B、用石墨电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、向CaCl2溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | ||||
| D、等物质的量浓度的小苏打溶液和石灰水按体积比3:2混合:3HCO3-+2Ca2++3OH-═2CaCO3↓+CO32-+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L CH3CHO中含有的分子数为NA |
| B、pH=1的稀硫酸中含有的H+数为0.1NA |
| C、7.80g Na2O2与5.85g NaCl所含阴离子数相等 |
| D、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
| B、制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| C、制乙烯时,用排水法或向上排空气法收集气体 |
| D、制二氧化氮时,用水或NaOH溶液吸收尾气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com