
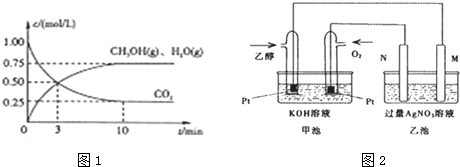
分析 I.(1)由图1可知,甲醇的浓度变化量为0.75mol/L,根据v=$\frac{△c}{△t}$计算v(CH3OH),再利用速率之比等于化学计量数之比计算v(H2);
(2)转化率=$\frac{浓度变化量}{起始浓度}$×100%;
(3)使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,改变条件使平衡向正反应移动,但只增大二氧化碳的浓度会使该比值减小;
Ⅱ.(1)碱性乙醇电池为原电池,通入乙醇的电极是负极,通入氧气的电极是正极,乙池有外接电源,属于电解池,N与原电池正极相连,则N是阳极,M与原电池负极相连,M为阴极,工作时M、N两个电极的质量都不减少,则Fe为阴极;
(2)原电池负极发生氧化反应,乙醇在负极失去电子,碱性条件下生成碳酸根离子与水;
(3)乙池中阴极发生反应:Ag++e-=Ag,阳极发生反应:2H2O+4e-=O2↑+4H+,根据电子转移守恒计算n(H+),计算溶液中c(H+),再根据pH=-lgc(H+)计算;
(4)计算1mol乙醇燃烧放出的热量,注明物质的聚集状态与反应热书写热化学方程式.
解答 解:(1)由图1可知,10min达平衡时甲醇的浓度变化量为0.75mol/L,所以v(CH3OH)=$\frac{0.75mol/L}{10min}$=0.075mol/(L•min),速率之比等于化学计量数之比,所以v(H2)=3v(CH3OH)=3×0.075mol/(L•min)=0.225mol/(L•min);
故答案为:0.225;
(2)平衡时二氧化碳的浓度变化量为1mol/L-0.25mol/L=0.75mol/L,故该条件下CO2的转化率为为$\frac{0.75mol/L}{1mol/L}$×100%=75%,
故答案为:75%;
(3)使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,改变条件使平衡向正反应移动,但只增大二氧化碳的浓度会使该比值减小
A.正反应为放热反应,升高温度,平衡向逆反应移动,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$减小,故A错误;
B.恒容时充入氮气,反应混合物的浓度不变,平衡不移动,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$不变,故B错误;
C.将H2O(g)从体系中分离,平衡向正反应移动,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,故C正确;
D.加入更有效的催化剂,平衡不移动,$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$不变,故D错误,
故选:C;
Ⅱ.(1)碱性乙醇电池为原电池,通入乙醇的电极是负极,通入氧气的电极是正极,乙池有外接电源,属于电解池,N与原电池正极相连,则N是阳极,M与原电池负极相连,M为阴极,工作时M、N两个电极的质量都不减少,则Fe为阴极,
故答案为:Fe;
(2)原电池负极发生氧化反应,乙醇在负极失去电子,碱性条件下生成碳酸根离子与水,电极反应式为:C2H5OH-12e+16OH-=2CO32-+11H2O,
故答案为:C2H5OH-12e+16OH-=2CO32-+11H2O;
(3)乙池中阴极发生反应:Ag++e-=Ag,析出Ag的物质的量为$\frac{4.32g}{108g/mol}$=0.04mol,阳极发生反应:2H2O+4e-=O2↑+4H+,根据电子转移守恒n(H+)=0.04mol,则c(H+)=$\frac{0.04mol}{0.4L}$=0.1mol/L,溶液pH=-lg0.1=1,
故答案为:1;
(4)1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,则1mol乙醇燃烧放出的热量=29.71kJ×$\frac{1mol×46g/mol}{1g}$=1366.66kJ,故热化学反应方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.66kJ/mol,
故答案为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1366.66kJ/mol.
点评 本题考查化学平衡计算与影响因素、电化学、热化学方程式书写等,属于拼合型题目,是对学生综合能力的考查,难度中等.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:填空题
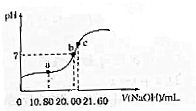 草酸(H2C2O4,二元酸弱)与草酸盐在实验和工业生产中都起着重要的作用.
草酸(H2C2O4,二元酸弱)与草酸盐在实验和工业生产中都起着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 Mpa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定它的碳、氢元素的质量比 | |
| B. | 只要证明它完全燃烧后产物有H2O和CO2 | |
| C. | 测定其产物中H2O和CO2的比值 | |
| D. | 测定该试样质量及试样完全燃烧后产物的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| B. | 向装有2mL 2mol/L AlCl3溶液的试管中,逐滴加入0.01mol/L氨水3mL,产生沉淀且沉淀不溶解,说明氢氧化铝不溶于弱碱 | |
| C. | 在淀粉溶液中加入稀硫酸并加热数分钟,冷却后依次加入新制Cu(OH)2悬浊液和碘水可检验淀粉是否已发生水解和是否完全水解 | |
| D. | 海带灼烧成灰烬后,加水煮沸2~3min并过滤,滤液中可加入适量的H2O2来氧化I? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com