
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.含有金属元素的晶体不一定是离子晶体 |
| B.原子晶体中只存在共价键 |
| C.HF、HC1、HBr、HI四种物质的沸点依次升高 |
| D.金属晶体之所以能导电是因为其中含有自由移动的电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成的难溶物是Cu(OH)2 |
| B.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤对电子 |
| C.沉淀溶解后将生成深蓝色的正四面体形的配离子[Cu(NH3)4]2+ |
| D.加入极性较小的溶剂乙醇后,将析出[Cu(H2O)4]SO4·H2O晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.PH3分子是极性分子 |
| B.PH3分子内二个价键的键氏和键能均相等 |
| C.PH3分子内=个P-H键的键长相等,键角均为93.6° |
| D.PH3分子内二个P-H键的键K相等,键角均为120° |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
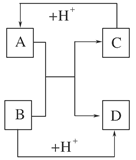
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子中3个原子的最外层电子数之和可能为21 |
| B.该分子的空间构型可能为折线型 |
| C.该分子可能是极性分子,也可能是非极性分子 |
| D.该分子中3个原子一定共平面 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.沉淀溶解后,生成深蓝色的配离子为[Cu(NH3)4]2+ |
| B.向反应后的溶液中加入乙醇,有沉淀析出 |
| C.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对 |
| D.反应前后,Cu2+浓度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
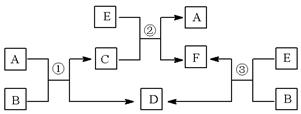
 D、E的循环。则B的电子式为_________________,反应①的离子方程式_____________________________。
D、E的循环。则B的电子式为_________________,反应①的离子方程式_____________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
 较,NH3 HF(选填“>”或“<”);
较,NH3 HF(选填“>”或“<”);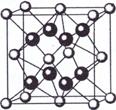
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com