
分析 X、Y、Z、W四种元素,前三种元素的离子结构都和氖原子具有相同的核外电子排布,X没有正价态,则X是F元素;Y的氢化物为H2Y,Y位于第VIA族,且Y离子与Ne原子核外电子排布相同,则Y是O元素;
0.2mol的Z原子能从酸中置换出2.24L H2(标准状况),氢气的物质的量是0.1mol,转移0.2mol电子,根据转移电子守恒知,0.2molZ转移0.2mol电子,所以Z为第IA族的Na元素;
W的原子核内没有中子,则W是H元素;
结合题目分析解答.
解答 解:X、Y、Z、W四种元素,前三种元素的离子结构都和氖原子具有相同的核外电子排布,X没有正价态,则X是F元素;Y的氢化物为H2Y,Y位于第VIA族,且Y离子与Ne原子核外电子排布相同,则Y是O元素;
0.2mol的Z原子能从酸中置换出2.24L H2(标准状况),氢气的物质的量是0.1mol,转移0.2mol电子,根据转移电子守恒知,0.2molZ转移0.2mol电子,所以Z为第IA族的Na元素;
W的原子核内没有中子,则W是H元素;
(1)通过以上分析知,X、Y、Z分别是氟、氧、钠元素,
故答案为:氟;氧;钠;
(2)Z是Na、X是F元素,二者通过得失电子形成离子化合物NaF,其形成过程为 ;氟化钠中只含离子键,所以属于离子化合物,
;氟化钠中只含离子键,所以属于离子化合物,
故答案为: ;离子化合物;离子键.
;离子化合物;离子键.
点评 本题考查位置结构性质相互关系及应用,为高频考点,涉及元素判断、化学键及化合物类型判断、用电子式表示化合物形成过程,注意电子式的表示方法,题目难度不大.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 1.6mol | C. | 2.2mol | D. | 2.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
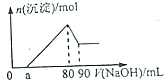 Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )
Fe2O3和Al2O3的混合物完全溶解于160mL2mol/LHCl溶液中,在所得溶液中滴加NaOH溶液得到如图,下列说法不正确的是( )| A. | 若a=20mL时,则混合物中Fe2O3占0.02mol | |
| B. | 所滴加的Na0H溶液的浓度为4mol/L | |
| C. | a点处,Na0H溶液的体积为a<50mL | |
| D. | 若a=20mL,则剩余盐酸的体积为20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | Ba(OH)2溶液 | D. | BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
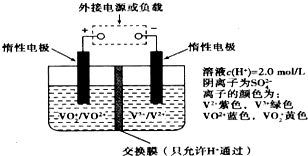 在能源和环保的压力下,新能源电动汽车无疑将成为未来汽车的发展方向.如果电动汽车上使用新型钒电池,一次性充电3-5分钟后,续航能力可达1000公里;而成本造价只有目前锂电池的40%,体积和重量分别是锂电池的$\frac{1}{25}$和$\frac{1}{10}$.全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示:下列有关该钒电池的说法不正确的是( )
在能源和环保的压力下,新能源电动汽车无疑将成为未来汽车的发展方向.如果电动汽车上使用新型钒电池,一次性充电3-5分钟后,续航能力可达1000公里;而成本造价只有目前锂电池的40%,体积和重量分别是锂电池的$\frac{1}{25}$和$\frac{1}{10}$.全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示:下列有关该钒电池的说法不正确的是( )| A. | 充电过程中,H+可以通过质子交换膜向右移动,形成电流通路,并且参与电极反应 | |
| B. | 放电过程中,右槽溶液中溶液颜色由紫色变为绿色 | |
| C. | 该电池为可逆电池,当左槽溶液逐渐由黄变蓝时,为充电过程,此时左槽溶液pH值升高 | |
| D. | 充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)增加了0.5mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com