
下列物质在水溶液状态下电离方程式错误的是
A.CaCO3 = Ca2++CO32— B.NaHSO4 = Na++HSO4—
C.H2CO3 H++HCO3— D.NH3·H2O
H++HCO3— D.NH3·H2O NH4++OH—
NH4++OH—
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
选择下列试验方法分离物质,将分离方法的序号填在横线上。
A 萃取分液法 B 加热分解 C 分液法 D 蒸馏法 E 过滤法
(1) 分离饱和食盐水与沙子的混合物
(2) 分离水和汽油的混合物
(3) 从碘的水溶液里提取碘
(4) 分离四氯化碳(沸点76.75℃)和甲苯(沸点110.6℃)的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中导电性最强的是
A.1L0.1mol/L醋酸 B.0.1L 0.1mol/L H2SO4溶液
C.0.5L 0.1mol/L盐酸 D.2L 0.1mol/L H2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,反应x A+yB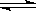 zC达到平衡:
zC达到平衡:
⑴若A、B、C均为气体,则该反应的平衡常数表达式为 ;
⑵若A、B、C均为气体,减压后平衡向逆反应方向移动,则x、y、z间的关系是 ;
⑶若已知C是气体,且x+y=z,在增大压强时,若平衡发生移动,则一定向 (填“正”或“逆”)反应方向移动;
⑷已知B、C是气体,当其他条件不变时,增大A的物质的量,平衡不移动,则A为 态;
⑸加热后C的质量分数减少,则正反应是 (填“放热”或“吸热”)反应。升高温度达到新的平衡后,该反应的平衡常数将变 (填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
250℃和1.01×105 Pa时, 2N2O5(g) = 4NO2(g) + O2(g) △H= +56.76 kJ/mol,该反应能自发进行的原因是
A.是吸热反应 B.是放热反应
C.是熵减少的反应 D.熵增大效应大于焓效应
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃,水的电离达到平衡: H2O H++OH-;H>0,下列叙述正确的是
H++OH-;H>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=13的氨水溶液稀释至10倍后pH=12
C.0.2 mol/L的盐酸与等体积水混合后pH=1
D.pH=12的氨水溶液与pH=2的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
现有如下各种说法:①在水中氢、氧原子间均以化学键相结合 ②硅晶体熔化需要克服分子间作用力 ③离子键是阳离子和阴离子的相互吸引力 ④根据电离方程式HCl===H++Cl-,判断HCl分子里存在离子键⑤有化学键断裂的变化属于化学变化。上述各种说法正确的是( )
A.都不正确 B.① ② ⑤ C.② ④ ⑤ D.① ② ③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com