
【题目】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1=-285.8 kJ/mol;
H2O(l) ΔH1=-285.8 kJ/mol;
②CO (g)+1/2O2 (g)![]() CO2 (g) ΔH2=-283kJ/mol
CO2 (g) ΔH2=-283kJ/mol
③CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
则工业制备甲醇的可逆反应热化学方程式为_______________________________;
(2)恒温恒容条件下,下列描述中能说明上述反应已达平衡状态的是__________。
A.单位时间内生成n mol CO的同时生成2n mol H2 B.ν(H2)正=2ν(CH3OH)逆
C.容器内气体的密度保持不变 D.容器中气体的压强保持不变
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,CO物质的量随时间变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
n(CO)/mol | 1.00 | 0.79 | 0.63 | 0.54 | 0.50 | 0.50 |
则从反应开始到20min时,以ν(H2)=________,该温度下平衡常数K=_______。
(4)加入催化剂后在250 ℃开始反应,CO的平衡转化率与温度、压强的关系如图所示。
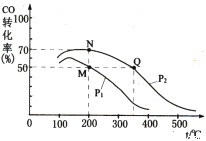
①M、N、Q三点的平衡常数KM、KN、KQ的大小关系为___________________________。
②由M点到N点改变的外界条件是_________。
A、降低温度 B、增大压强
C、改用更好的催化剂 D、通入更多的CO
(5)25℃时以稀硫酸为电解质溶液制成甲醇燃料电池,则负极的电极方程式为_________________________。
【答案】 CO(g)+2H2(g)![]() CH3OH(g)△H=-90 kJ/mol BD 0.025mol/(L·min) 4 (mol/L)-2 KM=KN>KQ B CH3OH-6e-+H2O
CH3OH(g)△H=-90 kJ/mol BD 0.025mol/(L·min) 4 (mol/L)-2 KM=KN>KQ B CH3OH-6e-+H2O![]() CO2↑+6H+
CO2↑+6H+
【解析】(1)反应①×2+反应②-反应③,得到:CO(g)+2H2(g)![]() CH3OH(g)△H=-90 kJ/mol。
CH3OH(g)△H=-90 kJ/mol。
(2)单位时间内生成n mol CO的同时生成2n mol H2,说的都是逆反应,没有说明正反应的情况,所以选项A不能说明反应达平衡。ν(H2)正=2ν(CH3OH)逆,说明了两个方向的速率,且速率比等于系数比,选项B能说明反应达平衡。根据质量守恒定律,总质量不变,总体积也不变,所以密度恒定不变,选项C不能说明反应达平衡。恒容下,容器中气体的压强保持不变,就是气体的物质的量不变,所以选项D能说明反应达平衡。
(3)![]() ,所以
,所以 ![]() = 0.025mol/(L·min)。根据题目数据可计算如下:
= 0.025mol/(L·min)。根据题目数据可计算如下:
CO(g) + 2H2(g)![]() CH3OH(g)
CH3OH(g)
起始: 1 2 0
反应: 0.5 1 0.5
平衡: 0.5 1 0.5
所以CO、H2和CH3OH的平衡浓度分别为:0.25mol/L、0.5mol/L和0.25mol/L,所以反应的平衡常数![]() (mol/L)-2。
(mol/L)-2。
(4)①由图得到M、N、Q三点的温度为:Q>M=N,因为反应放热,K值随温度上升而下降,所以M、N、Q三点的平衡常数KM、KN、KQ的大小关系为:KM=KN>KQ。
②题目中对该图的描述是:CO的平衡转化率与温度、压强的关系如图所示。图中横坐标是温度,表示温度对CO的平衡转化率的影响,所以两条曲线一定代表不同压强,以表示压强对于CO平衡转化率的影响。所以M到N必须变化压强,选项B正确。
(5)甲醇燃料电池的总反应为:CH3OH + 3/2O2 = CO2 + 2H2O,因为电解质为硫酸,所以正极反应为:O2 + 4H+ + 4e- = 2H2O,总反应减去正极反应(注意将正极反应扩大3/2倍),得到负极反应:CH3OH-6e-+H2O![]() CO2↑+6H+。
CO2↑+6H+。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铜与稀硫酸不发生反应,但如果在铜与稀硫酸的混合溶液中加入某种盐,就能发生反应, 且有气体、有沉淀产生,则该盐是 ( )
A.Ba(NO3)2B.KClC.Na2SO4D.FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列烃分子,完成填空。
①![]() ②
②  ③
③ 
④ ⑤
⑤ ![]() ⑥
⑥ 
(1)属于烷烃的有___________;互为同系物的有_____、______;(填序号)
(2)任写一种①的同分异构体的结构简式 ___________;
(3)④生成氯乙烷的反应方程式为:________________________;
(4)③在一定条件下与液溴反应方程式为:_______________________;
(5)②与水反应方程式为:________________________;
(6)④的二氯代物有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法不正确的是
A. 甲、乙、丙三种物质都含有氮元素 B. 反应Ⅱ、Ⅲ和Ⅳ的氧化剂相同
C. Ⅵ的产物可在上述流程中被再次利用 D. 丁为NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3mol O2加入到V L的反应器中,在高温下放电,经t1s建立了平衡体系:3O22O3 , 此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
A.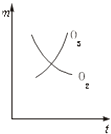
B.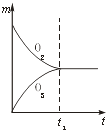
C.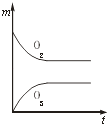
D.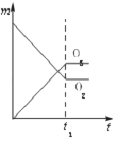
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体中能够降低血糖的激素和能促进生殖器官发育以及生殖细胞形成的激素的化学本质分别是 ( )
A.蛋白质和脂肪 B.脂质和蛋白质
C.蛋白质和固醇 D.磷脂和蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 澄清透明的溶液中: Fe3+、Mg2+、SCN-、Cl-
B. c(H+)/ c(OH-) = 1×10-12的溶液中:K+、Na +、CO32-、NO3-
C. c(Fe3+) =1 mol·L-1的溶液中: Na+、NH4+、AlO2-、SO42-
D. 能使甲基橙变红的溶液中: K+、NH4+、SO42-、HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com