
| A. | 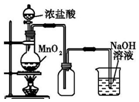 图中:如果MnO2过量,浓盐酸就可全部消耗 | |
| B. | 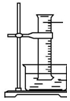 图中:如果倒置的量筒充满了氯气,水槽内装满水,经足够长的时间光照,量筒内最后剩余气体为HCl和氧气 | |
| C. | 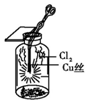 图中:生成蓝色的烟 | |
| D. | 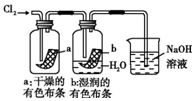 图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
分析 A.依据二氧化锰与盐酸反应的条件解答;
B.氯化氢极易溶于水;
C.铜与氯气反应生成棕黄色氯化铜;
D.依据起漂白作用的是次氯酸,结合氯气与水反应生成的氯化钠和次氯酸钠在酸性溶液中会发生归中反应判断解答;
解答 解:A.二氧化锰只与浓盐酸反应,与稀盐酸不反应,所以随着反应进行盐酸浓度降低变为稀盐酸,不再与二氧化锰反应,故A错误;
B.如果倒置的量筒充满了氯气,水槽内装满水,经足够长的时间光照,量筒内最后剩余气体为氧气,故B错误;
C.铜与氯气反应生成棕黄色氯化铜,产生大量棕黄色的烟,故C错误;
D.Ⅱ图中:湿润的有色布条能褪色,是因为氯气与水反应生成盐酸和次氯酸,次氯酸具有漂白性,使有色布条褪色,剩余氯气通入到盛氢氧化钠溶液的烧杯中发生反应为,Cl2+2NaOH=NaCl+NaClO+H2O,将硫酸溶液滴入烧杯中,至溶液显酸性,氯化钠和次氯酸钠会发生氧化还原反应,离子方程式为Cl-+ClO-+2H+=Cl2↑+H2O,所以结果有Cl2生成,故D正确;
故选D:
点评 本题考查了实验基本操作的装置、现象、原理,熟悉氯气制备原理和氯气的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量稀硫酸与少量锌反应,滴加少量 CuSO4 溶液,加快了反应速率,不影响 H2总量 | |
| B. | 足量的锌和少量稀硫酸反应,加入醋酸钠溶液降低反应速率,减少了生成的 H2总量 | |
| C. | 2-甲基丙烷光照下与氯气反应,得到 3 种一氯代物 | |
| D. | 仅用水就能鉴别酒精和己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
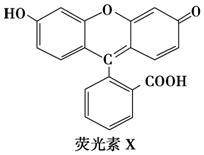
| A. | 1 mol X与足量的NaOH溶液在常温常压下反应,最多消耗3 mol NaOH | |
| B. | X能与糠醛( 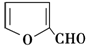 )发生缩聚反应 )发生缩聚反应 | |
| C. | 1 mol X与足量的浓溴水反应,最多消耗4 mol Br2 | |
| D. | 1 mol X最多能与9 mol氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅晶体是由SiO2分子构成的,它的熔点低、硬度大 | |
| B. | 由SiO2不能与水反应生成H2SiO3,可知SiO2不是H2SiO3的酸酐 | |
| C. | 将硫酸和碳酸钠反应产生的气体通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3 | |
| D. | SiO2既能与NaOH溶液反应又能与氢氟酸反应,所以SiO2是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同状况下两电极上产生的气体体积之比为2:1 | |
| B. | 两电极上产生的气体质量之比为8:1 | |
| C. | 相同状况下两电极上产生的气体体积之比为4:1 | |
| D. | 若两电极上产生的气体质量比为16:3,则D2O与H2O的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
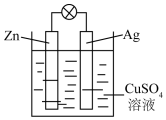 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.
如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
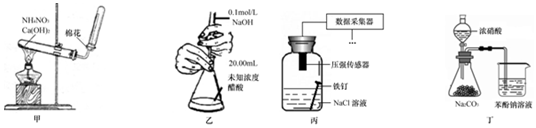
| A. | 用甲装置制取氨气 | |
| B. | 用乙装置测定醋酸浓度 | |
| C. | 用丙装置采集到的压强数据判断铁钉发生电化学腐蚀类型 | |
| D. | 用丁装置验证酸性:硝酸>碳酸>苯酚 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com