
【题目】工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示:
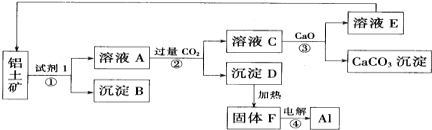
(1)试剂1为______(填化学式),①~④转化过程中_____消耗能量最多。
(2)沉淀B的化学式为______。
(3)电解F,当转移6mol电子时,可制得铝______ g。
(4)生产过程中,除物质E可以循环使用外,还可以循环使用的物质有______(填化学式)。
(5)写出离子方程式:①______, ② ______。
(6)写出化学方程式:④______。
【答案】(1)NaOH;④;(2)Fe2O3;(3)54;(4)CaO和CO2;(5)① Al2O3+2OH- =2AlO2-+ H2O
② CO2+AlO2-+2H2O=Al(OH) 3↓+HCO3- (6)2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
【解析】
试题分析:(1)铝土矿(主要成分含氧化铝、氧化铁)加入氢氧化钠,氧化铁不和碱反应,氧化铝可与氢氧化钠反应生成偏铝酸钠和水;电解氧化铝需要破坏离子键,需要吸收大量的能量;
(2)铝土矿(主要成分含氧化铝、氧化铁)加入氢氧化钠,氧化铁不和碱反应,氧化铝可与氢氧化钠反应生成偏铝酸钠和水;过滤后得到的沉淀为氧化铁;
(3)电解氧化铝的方程式为2Al2O3![]() 4Al+3O2↑,设得到铝的质量为x,
4Al+3O2↑,设得到铝的质量为x,
2Al2O3![]() 4Al+3O2↑ 转移电子
4Al+3O2↑ 转移电子
108g 12mol
x 6mol
解得x=54g;
(4)煅烧碳酸钙得到CaO和CO2,B生成沉淀需要二氧化碳、碳酸钠转化为碳酸钙需要CaO,所以CaO和CO2能循环利用;
(5)偏铝酸钠溶液通入过量的二氧化碳反应生成氢氧化铝和碳酸氢钠,离子方程式为CO2+AlO2-+2H2O=Al(OH) 3↓+HCO3-;
(6)电解熔融氧化铝的方程式为2Al2O3![]() 4Al+3O2↑。
4Al+3O2↑。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列物质按纯净物、混合物、强弱电解质和非电解质顺序排列的是
A.单甘油酯、混甘油酯、苛性钾、H2S、三氧化硫
B.胆矾、漂白粉、硫酸钠、次氯酸、氯气
C.明矾、水煤气、盐酸、醋酸、铜
D.冰醋酸、福尔马林、硫酸钡、H2S、乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成抗心律失常药物决奈达隆的一种中间体,可通过以下方法合成:

(1)D中的含氧官能团名称为____________(写两种)。
(2)F→G的反应类型为___________。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:_________。
①能发生银镜反应;②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(4)E经还原得到F,E的分子是为C14H17O3N,写出E的结构简式:___________。
(5)已知:①苯胺(![]() )易被氧化
)易被氧化
②
请以甲苯和(CH3CO)2O为原料制备 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验室用如图所示装置制取少量溴苯。请填写下列空白。

(1)在烧瓶a中装的试剂是苯、溴和铁屑。导管b的作用有两个:一是导气,二是兼起_______的作用。
(2)反应过程中在导管c的下口附近可以观察到白雾出现,这是由于反应生成的________遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有________生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有褐色不溶于水的液体。这是溶解了溴的粗溴苯,可选用试剂 除去。
(5)写出烧瓶a中发生反应的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.除去乙醇中微量水用金属钠
B.溴苯中混有溴,加入水萃取
C.用酸性高锰酸钾除去乙烷中的乙烯
D.除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:(除特别注明外,其它一律用化学式表示)
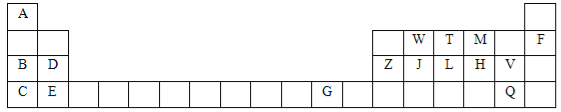
(1)化学性质最不活泼的单质是 ,最高价氧化物水化物中碱性最强的是 。
(2)J在周期表中的位置第 。
(3)某元素二价阳离子的核外有10个电子,该元素名称是 。
(4)M、H形成的气态氢化物的沸点比较: (用 > 连接)。
(5)写出工业合成T的气态氢化物的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。

(1)乙醇分子官能团名称是_______________。
(2)试管a中加入几块碎瓷片的目的是___________。
(3)试管a中发生反应的化学方程式为 ___________,反应类型是_______。
(4)可用_________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油化工的重要原料,它主要通过石油产品裂解获得。
(1)石油产品裂解所得裂解气的平均组成可表示为CnHm(m>2n),经测定某裂解气中各气体的体积分数分别为:甲烷―4%、乙烯―50%、丙烯―10%、其余为丁二烯和氢气(气体体积均在同温同压下测定)。若得到50 mol乙烯,x mol丁二烯和y mol氢气。则x+y= , n / m = (请用含x的式子表示)。(4分)
(2)某化工厂每天由石油产品裂解得到乙烯56 t。再以乙烯为主要原料生产醋酸乙烯酯,醋酸乙烯酯是合成维尼纶的重要单体。生产原理如下:

反应①中乙烯的利用率为80%,反应②中乙醛的利用率为83.33%,反应③中乙酸与乙烯的利用率均为85%。则该厂每天最多可制得醋酸乙烯酯多少吨?(8分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为4种短周期元素。已知:①X、W同主族,Y、Z同主族;②X、Y可形成两种液态化合物X2Y和X2Y2;③X2Z和ZY2之间可发生反应生成Z单质;④W2Y2和X2Y之间可发生反应生成Y单质。
请完成下列问题:
(1)X、Y元素的名称为X________,Y________。
(2)写出W2Y2的电子式:__________,Z的原子结构示意图为__________。
(3)写出④ 中反应的化学方程式__ ___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com