
【题目】PAFC{聚合碱式氯化铝铁,通式:[FeaAlb(OH)xCly]n}是一种新型的无机高分子絮凝剂.以高铁铝土矿、硫酸厂渣尘为配料(主要成分:Al2O3、Fe2O3 , 杂质FeO、SiO2等)为原料制取PAFC的实验流程如下: 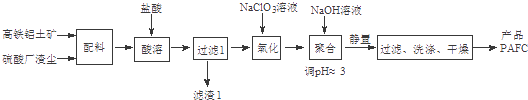
(1)为提高“酸溶”速率,除适当增大盐酸浓度外,还可采取的措施有(举一例).
(2)“酸溶”时,Al2O3与盐酸反应的化学方程式为 , 滤渣1的主要成分为(写化学式)
(3)“氧化”时,NaClO3氧化Fe2+ , 本身被还原为Cl﹣ , 该反应的离子方程式为 .
(4)“聚合”时,若将溶液pH调得过高,可能造成的影响是 .
(5)![]() 是衡量PAFC净水效果的重要参数之一,某合作学习小组的同学拟通过实验确定产品中
是衡量PAFC净水效果的重要参数之一,某合作学习小组的同学拟通过实验确定产品中 ![]() 的比值. 步骤1.准确称取5.710g样品,溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.350g固体.
的比值. 步骤1.准确称取5.710g样品,溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.350g固体.
步骤2.另准确称取2.855g样品,溶于足量NaOH溶液,过滤,充分洗涤,将滤渣灼烧至质量不再变化,得到固体0.4000g.
①通式[FeaAlb(OH)xCly]n中,a、b、x、y的代数关系式为
②产品中n(Al)/n(Fe)的比值为 .
【答案】
(1)升高反应温度或减少固体配料的粒直径
(2)Al2O3+6HCl=2AlCl3+3H2O;SiO2
(3)ClO3﹣+6Fe2++6H+=Cl﹣+6Fe3++3H2O
(4)铁转化为Fe(OH)3沉淀,铝转化为Al(OH)3或AlO2﹣
(5)3a+3b=x+y;5:1
【解析】解:(1)根据影响反应速率的因素可知,为提高“酸溶”速率可采取的措施是升高反应温度或减少固体配料的粒直径, 所以答案是:升高反应温度或减少固体配料的粒直径;(2)Al2O3与盐酸反应生成氯化铝和水,反应的方程式为Al2O3+6HCl=2AlCl3+3H2O,根据上面的分析可知滤渣1的主要成份为SiO2 ,
所以答案是:Al2O3+6HCl=2AlCl3+3H2O;SiO2;(3)NaClO3氧化Fe2+ , 本身被还原为Cl﹣ , 反应的离子方程式为ClO3﹣+6Fe2++6H+=Cl﹣+6Fe3++3H2O,
所以答案是:ClO3﹣+6Fe2++6H+=Cl﹣+6Fe3++3H2O;(4)根据铁离子和铝离子的性质可知,如果溶液的pH值过高,则会生成氢氧化铁沉淀和偏铝酸盐,
所以答案是:铁转化为Fe(OH)3沉淀,铝转化为Al(OH)3或AlO2﹣;(5)①根据化合物中元素的化合价为零可得关系式3a+3b=x+y,
所以答案是:3a+3b=x+y;②根据题意,由步骤2 在2.855g样品中:160gmol﹣1×n(Fe2O3)=0.4000g,n(Fe2O3)=0.0025mol,相当于5.710g样品中含n(Fe2O3)=0.0050mol,
由步骤1在5.710g样品中:102gmol﹣1×n(Al2O3)+160gmol﹣1×n(Fe2O3)=3.350g;102gmol﹣1×n(Al2O3)=3.350g﹣2×0.4000g,所以n(Al2O3)=0.025mol
则n(Al)/n(Fe)= ![]() =5:1,
=5:1,
所以答案是:5:1.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于氯气和氯水的说法中正确的是( )
A. 氯气是一种无色、密度比空气大的有毒气体
B. 新制氯水保存在无色试剂瓶中
C. 新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌
D. 氯水放置数天后酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国外宇航员吃着“牙膏和砖块”时,中国宇航员已经在太空泡茶了,每个茶装在特制包装袋中,注水后用加热器进行加热就可以喝了,但要插上吸管以防止水珠飘起来。下列说法正确的是( )
物质 | 氧化镁 | 氯化镁 |
熔点/℃ | 2 852 | 714 |
A. 宇航员喝茶时注入的H2O的摩尔质量是18克
B. H2O+Cl2![]() HCl+HClO这反应属于氧化还原反应
HCl+HClO这反应属于氧化还原反应
C. 氢的三种同位素1H、2D、3T与16O只能形成三种水分子
D. 在标准状况下,1mol水的体积约是22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见物质之间的转化如下图所示:
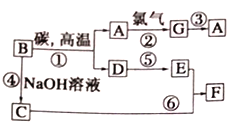
其中B常被用于制造光导纤维,其对应的单质的结构与金刚石的结构是相似的。
(1)试推测:A______,F___________(写化学式)
(2)试写出反应④的离子方租式:__________。
(3)写出反应①的化学方程式____________。
(4)在反应①中,碳的作用是______,当生成1molA时,转移电子的数目为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苦杏仁酸(D)是一种重要的医药中间体,可通过下列方法合成: 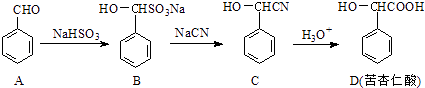
①A→B的反应类型为
②D能缩聚为聚酯,聚酯的结构简式为
③E是D的同分异构体,E中含有苯环,且E能发生如下水解反应:E+H2O ![]() CH3OH+F符合条件的F的结构种,其中核磁共振氢谱有4组峰且面积比为1:2:2:1的结构简式为 .
CH3OH+F符合条件的F的结构种,其中核磁共振氢谱有4组峰且面积比为1:2:2:1的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据反应原理设计的应用,不正确的是( )
A.CO ![]() +H2O?HCO
+H2O?HCO ![]() +OH﹣;用热的纯碱溶液清洗油污
+OH﹣;用热的纯碱溶液清洗油污
B.Al3++3H2O?Al(OH)3(胶体)+3H+;明矾净水
C.TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl;制备TiO2纳米粉
D.SnCl2+H2O?Sn(OH)Cl↓+HCl;配制氯化亚锡溶液时加入氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成的实验是( )
①检验自来水中是否含有Cl- ②鉴别食盐和小苏打 ③蛋壳能否溶于酸 ④白酒中是否有甲醇
A.①②
B.①④
C.②③
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H、C、N、O、Al、S是常见的六种元素.完成下列填空:
(1)碳元素有12C、13C和14C等同位素.在14C原子中,核外存在对自旋相反的电子.
(2)碳在形成化合物时,其所成化学键以共价键为主,原因是 .
(3)任选上述元素可组成多种四原子的共价化合物,请写出其中含非极性键的一种化合物的电子式 .
(4)上述元素可组成盐NH4Al(SO4)2 . 向10mL1mol/L NH4Al(SO4)2溶液中滴加1mol/L的NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下.
①NH4Al(SO4)2溶液中所有离子的浓度由大到小的顺序是 , 请解释阳离子浓度差异的原因 .
②写出N点反应的离子方程式 .
③若向10mL1mol/L NH4Al(SO4)2溶液中加入20mL1.2mol/LBa(OH)2溶液,充分反应后,产生沉淀mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写错误的是
A.钠与水反应:2Na+2H2O===2Na++2OH+H2↑
B.适量钠与CuSO4溶液反应:2Na+Cu2+===Cu+2Na+
C.适量钠与盐酸反应:2Na+2H+===2Na++H2↑
D.适量钠跟氯化钾溶液反应:2Na+2H2O===2Na++2OH+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com