
【题目】某同学用图所示的装置及药品进行酸性强弱比较的实验,下列说法正确的是

A. ①和②中发生的反应均为氧化还原反应
B. 向Na2SiO3饱和溶液中滴酚酞溶液无明显现象
C. 一段时间后②中有胶冻状物质生成
D. 该实验能证明酸性强弱的顺序是:碳酸>硫酸>硅酸
【答案】C
【解析】
稀硫酸与碳酸钠反应生成二氧化碳气体,证明硫酸的酸性大于碳酸;将生成的二氧化碳气体通入硅酸钠溶液中,会观察到有白色胶状物,反应生成了硅酸胶体,证明了酸性:碳酸>硅酸,据此进行解答。
A.①中硫酸与碳酸钠反应生成硫酸钠、二氧化碳气体和水,②中二氧化碳与硅酸钠反应生成硅酸和碳酸钠,都不存在元素化合价升降,不是氧化还原反应,故A错误;
B.硅酸钠溶液呈碱性,所以向Na2SiO3饱和溶液中滴酚酞溶液后会显示红色,故B错误;
C.一段时间后②中生成硅酸胶体,则有胶冻状物质生成,故C正确;
D.稀硫酸与碳酸钠反应生成二氧化碳,证明酸性:硫酸>碳酸;将生成的二氧化碳气体通入硅酸钠溶液中,会观察到有白色胶状物,反应生成了硅酸胶体,证明酸性:碳酸>硅酸,该实验能证明酸性强弱的顺序是:硫酸>碳酸>硅酸,故D错误;
故答案为C。


科目:高中化学 来源: 题型:
【题目】秋冬季是雾霾高发季节,其中汽车尾气和燃煤尾气是造成雾霾的主要原因之一。
(1)工业上利用甲烷催化还原NOX可减少氮氧化物的排放。已知:
CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol
4NO(g)+CO2(g)+2H2O(g)△H=-574kJ/mol
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ/mol
2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为_______________________________。
(2)汽车尾气催化净化是控制汽车尾气排放、减少汽车尾气污染的最有效的手段,主要原理为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)△H<O。向一定条件下的恒容密闭容器中充入NO和CO,用传感器测得该反应在不同时刻NO和CO的浓度如下表所示:
N2(g)+2CO2(g)△H<O。向一定条件下的恒容密闭容器中充入NO和CO,用传感器测得该反应在不同时刻NO和CO的浓度如下表所示:
时间/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/mol·L-1 | 9.00×10-3 | 4.00×10-3 | 2.00×10-3 | 1.00×10-3 | 1.00×10-3 |
c(CO)/mol·L-1 | 9.00×10-3 | 4.00×10-3 | 2.00×10-3 | 1.00×10-3 | 1.00×10-3 |
①下列可判断反应达到平衡状态的是___________(填字母代号)。
A.c(NO)不再改变 B.c(NO)/c(CO)不再改变
C.c(NO)/c(CO2)不再改变 D.V(CO)=V(CO2)
②此条件下达到平衡时,计算该反应的平衡常数K=________。
③为了提高尾气处理的效果,可采取的措施有_____________________(写出两种即可)。
(3)工业上常采用“碱溶液吸收”的方法来同时吸收SO2和氮的氧化物气体(NOx),请写出氢氧化钠溶液吸收NO和NO2(两者体积比1:1)的离子方程式 ___________________。
(4)铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态。雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(两者物质的量之比为1:1)。可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如下图所示。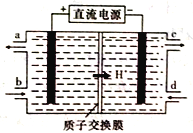
①Ce4+从电解槽的_____(填字母代号)口流出。
②写出阴极的电极反应式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:
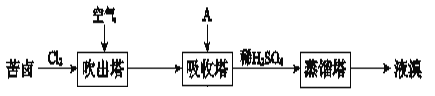
(1)Cl2和苦卤中的Br﹣反应生成Br2的离子方程式是_____。
(2)结合元素周期律解释Cl的非金属性强于Br的原因:_____。
(3)吸收塔中,A吸收了Br2后的溶液中含有Br﹣和BrO3﹣,则A是_____(填序号)。
a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
(4)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与环境保护、建筑材料、人体健康息息相关。
(1)2015年冬季我国出现大范围雾霾天气,许多城市发布PM2.5重度污染警报。
①下列行为不会增加城市大气中PM2.5浓度的是______(填序号)。
a.燃放烟花爆竹
b.露天焚烧落叶
c.为城市主干道洒水保洁
②燃煤气化有助于减少PM2.5,写出焦炭与水蒸气反应的化学方程式______________________________。
(2)材料是人类赖以生存和发展的重要物质基础。
①下列材料属于塑料的是______(填序号)。
a.钢化玻璃 b.有机玻璃 c.石英玻璃
②金刚石俗称钻石,它的主要成分是________(填序号)。
a.C b.SiO2 c.Al2O3
③生产硅酸盐水泥和普通玻璃都需用到的共同原料是____(填序号)。
a.石灰石 b.纯碱 c.黏土 d.石英
(3)药店中常用药品很多,如a.碘酒,b.青霉素,c.阿司匹林,d.胃舒平(含氢氧化铝)。
①碘酒是__________(填“纯净物”或“混合物”)。
②在使用前一定要进行皮肤敏感试验(皮试)的是______(填序号)。
③用离子方程式解释胃舒平可作为抗酸药的原因:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A. υ(CO)=1.5 mol·L-1·min-1 B. υ(NO2)=0.7 mol·L-1·min-1
C. υ(N2)=0.4 mol·L-1·min-1 D. υ(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 一定条件下SiO2可与碱和氢氟酸反应,故其属于两性氧化物
B. 制玻璃、水泥的原料都用到石灰石
C. 硅在常温下不与氧气、氯气、硝酸反应
D. 沙子、石英、水晶的主要成分都是SiO2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验及现象能推出相应结论的是
选项 | 实验操作 | 现象 | 结论 |
A | 向苯酚钠溶液中加入NaHSO3溶液 | 溶液变浑浊 | 酸性:H2SO3>苯酚 |
B | 向KI淀粉溶液中滴入无色溶液X | 溶液变蓝色 | X一定为H2O2溶液 |
C | 将3体积SO2与1体积O2混合并通过灼热的催化剂充分反应,产物依次通过BaCl2溶液和品红溶液 | 前者产生白色沉淀,后者溶液褪色 | SO2与O2的反应为可逆反应 |
D | 向2支均盛有2mL1.0mol·L-1的KOH溶液的试管中,分别加入2滴浓度均为0.1mol·L-1的AlCl3和FeCl3溶液 | 一支试管出现红褐色沉淀,另一支无明显现象 | Ksp[Al(OH)3]> Ksp[Fe(OH)3] |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气压强对许多物理实验和化学实验有着重要影响,制取氨气并完成喷泉实验。
图1 图2
图2
(1)检验圆底烧瓶中氨气收集满的方法是_________________________________。
(2)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是________,该实验的原理是________________________________________。
(3)如果只提供如图2的装置,请说明引发喷泉的方法:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯为原料合成一些化工产品的转化关系如下:

回答下列问题:
(1)A的名称是_________。
(2)C的结构简式为__________。
(3)B→D的反应类型是______;E中所含官能团名称是______。
(4)B→A的化学方程式为_________。
(5)写出E发生加聚反应方裎式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com