
| A. | 乙醇与乙酸在浓硫酸加热条件下反应 | |
| B. | 乙烯通入溴的四氯化碳溶液 | |
| C. | 苯与浓硝酸、浓硫酸的混合物共热 | |
| D. | 乙醇在铜粉存在下与氧气反应 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH3+Cl2$\stackrel{高温}{→}$CH2=CHCH2Cl+HCl 加成反应 | |
| B. | 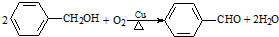 氧化反应 氧化反应 | |
| C. |  加成反应 加成反应 | |
| D. | 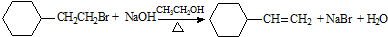 取代反应 取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;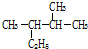 用系统命名法命名为2,3-二甲基戊烷;
用系统命名法命名为2,3-二甲基戊烷;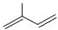 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标况下,22.4L SO3和22.4L C2H4原子个数比为2:3 | |
| B. | 将78g Na2O2与过量CO2反应,CO2转移的电子数为2NA | |
| C. | 含0.2mol H2SO4的浓硫酸与足量铜充分反应,生成SO2分子的数目少于0.1NA | |
| D. | 电解精炼铜时,若阳极质量减少32g,则阴极转移的电子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为53 | B. | 中子数为53 | C. | 质子数为131 | D. | 中子数为131 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
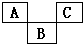 如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.回答:
如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.回答: ;B的最高价氧化物对应化物的化学式为H2SO4.
;B的最高价氧化物对应化物的化学式为H2SO4.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
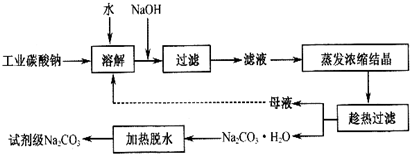
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题:
某学生实验小组,用稀硫酸和稀氢氧化钠溶液在如图所示的装置中,进行中和反应反应热的测定.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com