
| A、少量二氧化碳通入水玻璃中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ |
| B、钠投入水中:Na+H2O═Na++OH-+H2↑ |
| C、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
| D、氯气通入水中:Cl2+H2O═2H++Cl-+ClO- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| t/℃ | 700 | 800 | 900 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.3 | 1.8 | 2.7 |
| A、该反应正反应为放热反应 |
| B、起始浓度不变,K越大,反应物的转化率越大 |
| C、温度不变,增加X的用量,K增大 |
| D、达平衡后,加入催化剂,K增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液中:Na+、Cu2+、Cl-、NO3- |
| B、强酸性溶液中:Na+、K+、OH-、SiO32- |
| C、含Fe3+的溶液中:K+、Ca2+、NO3-、SCN- |
| D、澄清透明溶液中:Fe2+、Na+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清透明溶液:H+、Na+、SO42-、C6H5O- | ||
B、常温下
| ||
| C、铁片加入产生气泡的溶液:Na+、NH4+、I-、NO2- | ||
| D、NaHCO3溶液:K+、Na+、SO42-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
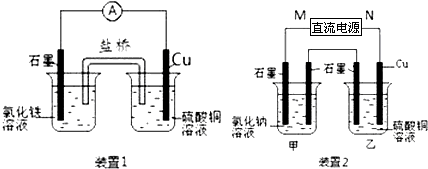
查看答案和解析>>
科目:高中化学 来源: 题型:
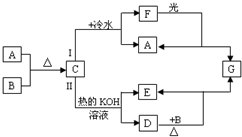 下列框图中A-G均为中学化学中常见的物质,除B、G外均含有同一种元素,D中该元素的化合价为+5.其中A、F为酸,D、E为盐,C、G为气体,其它反应产物略去.
下列框图中A-G均为中学化学中常见的物质,除B、G外均含有同一种元素,D中该元素的化合价为+5.其中A、F为酸,D、E为盐,C、G为气体,其它反应产物略去.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com