
关于选项中关于硝酸的说法正确的是
A.硝酸与金属反应时,不会表现出酸性
B.浓硝酸与浓盐酸按1:3的体积比所得的混合物叫王水
C.硝酸电离出的H+离子,能被锌、铁等金属还原成H2
D.常温下,向浓硝酸中投入铁片,会产生大量的红棕色气体
科目:高中化学 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:简答题
砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人类认识它、研究它的历史却很长。
(1)已知H3AsO3是两性偏酸性的化合物,H3AsO3中As的化合价为_____,它与足量硫酸反应时生成盐的化学式为_______________。Na2HAsO3溶液呈碱性,原因是_________________(用离子方程式表示),该溶液中c(H2AsO3-) _____c(AsO33-)(填”>”、“<”或“=”)。
(2)砷在自然界中主要以硫化物形式(如雄黄As4S4、雌黄As2S3等)存在。
①工业上以雄黄为原料制备砷、鉴定砒霜(As2O3)的原理如下图:

反应a产生的废气直接排放可能带来的环境问题是__________ _____,请写出反应b的化学方程式:_________________________。
②雌黄可被浓硝酸氧化为H3AsO4与S,硝酸被还原为NO2,反应中还原剂与氧化剂物质的量之比为_________。
③向c(As3+)=0.01mol/L的工业废水中加入FeS固体至砷完恰好完全除去(小于1×10-5mol/L),则此时c(Fe2+)=_____mol/L。(已知Ksp(As2S3)=1×10-22,Ksp(FeS)=6×10-18)
(3)某原电池装置如右图,电池总反应为AsO43-+2I-+H2O AsO33-+I2+2OH-当P池中溶液由无色变成蓝色时,正极上的电极反应式为_______________。当电流计指针归中后向Q池中加入一定量的NaOH,则电子由_____(填“P”或“Q”)池流出。
AsO33-+I2+2OH-当P池中溶液由无色变成蓝色时,正极上的电极反应式为_______________。当电流计指针归中后向Q池中加入一定量的NaOH,则电子由_____(填“P”或“Q”)池流出。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
人们把食品分为绿色食品、蓝色食品、白色食品等。绿色植物通过光合作用转化的食品叫绿色食品,海洋提供的食品叫蓝色食品,通过微生物发酵制得的食品叫白色食品。下面属于白色食品的是( )
A.酱油 B.面粉 C.海带 D.菜油
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.离子化合物中,阴、阳离子间存在静电吸引力
B.HF、HCl、HBr和HI的热稳定性和还原性从左到右依次减弱
C.第三周期非金属元素对应的含氧酸从左到右依次增强
D.短周期元素形成离子后,最外层电子数都达到8电子稳定结构
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
有一种MCPC型燃料电池,该电池所用燃料为H2和空气,电解质为熔融的K2CO3。电池的总反应为:2H2 + O2 = 2H2O,负极反应为H2 + CO32—-2e-= H2O + CO2。下列说法中正确的是
A.正极反应为4OH--4e-= 2H2O + O2↑
B.放电时,电池中CO32-的物质的量将逐渐减少
C.放电时CO32-向负极移动
D.电路中的电子经正极、负极、熔融的K2CO3后再流回正极,形成闭合回路
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:填空题
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ∆H <0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ∆H <0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ∆H <0 (Ⅱ)
2ClNO(g) K2 ∆H <0 (Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向 2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则:平衡后n(Cl2)= mol,NO的转化率а1= ,其它条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是 。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得 1L溶液A,溶液B为0.1mol•L?1的CH3COONa溶液,则两溶液中c(NO3?)、c(NO2-)和c(CH3COO?)由大到小的顺序为 。(已知HNO2的电离常数Ka=7.1×10-4mol•L?1,CH3COOH的电离常数Ka=1.7×10-5mol•L?1)。
可使溶液A和溶液B的pH相等的方法是 。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
在容积为2 L的3个密闭容器中发生反应3A(g)+B(g) 2C(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2C(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 3 mol A、2 mol B | 6 mol A、4 mol B | 2 mol C |
到达平衡的时间(min) | 5 | 8 | |
平衡时B的浓度( mol/L) | c1 | 1.5 | |
C的体积分数 | w1 | w2 | |
混合气体密度(g/L) | ρ1 | ρ2 |
下列说法不正确的是
A.容器乙中反应从开始到达平衡的反应速率为v(A)=0.3mol·L-1·min-1
B.2c1<1.5
C.2ρ1=ρ2
D.在该温度下甲容器中的反应平衡常数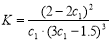
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三5月四模化学试卷(解析版) 题型:实验题
直接氧化法制备混凝剂聚合硫酸铁[Fe2(OH)n(SO4)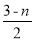 ]m(n>2,m≤10)的实验流程如下:
]m(n>2,m≤10)的实验流程如下:

已知:盐基度=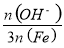 ×100%.式中n(OH-)、n(Fe)分别表示PFS中OH-和Fe3+的物质的量.所得产品若要用于饮用水处理,需达到盐基度指标为 8.0%~16.0%.
×100%.式中n(OH-)、n(Fe)分别表示PFS中OH-和Fe3+的物质的量.所得产品若要用于饮用水处理,需达到盐基度指标为 8.0%~16.0%.
(1)实验加入硫酸的作用是____________,取样分析Fe2+浓度,其目的是____________。
(2)用pH试纸测定溶液pH的操作方法为____________,若溶液的pH偏小,将导致聚合硫酸铁中铁的质量分数____________(填“偏高”、“偏低”、“无影响”)
(3)聚合反应的原理为m[Fe2(OH)n(SO4) 3-n/2]?[Fe2(OH)n(SO4)3-n/2]m,则水解反应的化学方程式为____________.
(4)产品盐基度的测定方法:
Ⅰ称取m g固体试样,置于400mL聚乙烯烧杯中,加入25mL盐酸标准溶液,再加20mL煮沸后冷却的蒸馏水,摇匀,盖上表面皿.
Ⅱ室温下放置10min,再加入10mL氟化钾溶液,摇匀,掩蔽Fe3+,形成白色沉淀.
Ⅲ加入5滴酚酞指示剂,立即用物质的量浓度为c mol•L-1的氢氧化钠标准液滴定至终点,消耗体积为VmL.
Ⅳ向聚乙烯烧杯中,加入25mL盐酸标准溶液,再加20mL煮沸后冷却的蒸馏水,摇匀,盖上表面皿.然后重复Ⅱ、Ⅲ做空白试验,消耗氢氧化钠标准液的体积为V0mL.
①达到滴定终点的现象为____________。
②已知试样中Fe3+的质量分数为w1,则该试样的盐基度(w)的计算表达式为____________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄冈市高三5月一模理综化学试卷(解析版) 题型:选择题
下列古诗中对应的化学物质及相关说法均正确的是( )
选项 | 诗句 | 相关物质 | 相关说法 |
A | 春蚕到死丝方尽 | 纤维素 | 高分子化合物 |
B | 蜡炬成灰泪始干 | 脂肪烃 | 不饱和烃 |
C | 沧海月明珠有泪 | 碳酸钙 | 强电解质 |
D | 蓝田日暖玉生烟 | 二氧化硅 | 两性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com