
 .
. +2NaOH$\stackrel{一定条件}{→}$
+2NaOH$\stackrel{一定条件}{→}$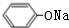 +NaBr+H2O.
+NaBr+H2O.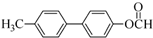 .
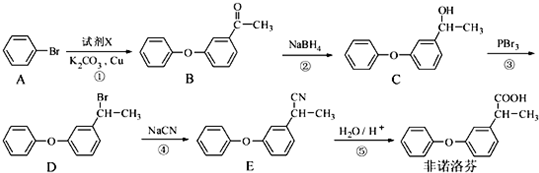
.分析 (1)根据B的结构简式可知,含有的氧官能团为羰基、醚键;
(2)对比A、B的结构可知,应是发生取代反应,据此判断X的结构简式;
(3)对比B、C结构可知,B中羰基被还原为羟基;对比D、E结构可知,D中-Br被-CN取代生成E;
(4)溴苯在氢氧化钠水溶液发生水解反应得到苯酚与HBr,而苯酚、HBr由于氢氧化钠反应得到苯酚钠、NaBr;
(5)B的一种同分异构体满足下列条件:Ⅰ.能发生银镜反应,说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应,含有甲酸与酚形成的酯基(-OOCH);Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环,苯环通过碳碳单键相连,甲基与-CHO处于对位;
(6)a.根据非诺洛芬的结构简式确定其分子式;
b.非诺洛芬含有羧基、苯环,可以发生取代反应;
c.苯环与氢气发生加成反应;
d.苯环中含有1个大π键,羧基中含有1个π键.
解答 解:(1)根据B的结构简式可知,含有的氧官能团为羰基、醚键,故答案为:羰基、醚键;
(2)对比A、B的结构可知,应是发生取代反应,可推知X的结构简式为 ,故答案为:
,故答案为: ;
;
(3)对比B、C结构可知,B中羰基被还原为羟基,属于还原反应,对比D、E结构可知,D中-Br被-CN取代生成E,属于取代反应,故答案为:还原反应;取代反应;
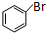
(4)A的名称为溴苯,溴苯在氢氧化钠水溶液发生水解反应得到苯酚与HBr,而苯酚、HBr由于氢氧化钠反应得到苯酚钠、NaBr,反应方程式为: +2NaOH$\stackrel{一定条件}{→}$
+2NaOH$\stackrel{一定条件}{→}$ +NaBr+H2O,
+NaBr+H2O,
故答案为:溴苯; +2NaOH$\stackrel{一定条件}{→}$
+2NaOH$\stackrel{一定条件}{→}$ +NaBr+H2O;
+NaBr+H2O;
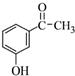
(5)B的一种同分异构体满足下列条件:Ⅰ.能发生银镜反应,说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应,含有甲酸与酚形成的酯基(-OOCH);Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环,苯环通过碳碳单键相连,甲基与-CHO处于对位,该同分异构体的结构简式为 ,故答案为:
,故答案为: ;
;
(6)a.根据非诺洛芬的结构简式,可知其分子式为C15H14O3,故a错误;
b.非诺洛芬含有羧基、苯环,可以发生取代反应,故b正确;
c.苯环与氢气发生加成反应,1mol非诺洛芬最多可以和6molH2发生加成反应,故c正确;
d.苯环中含有1个大π键,羧基中含有1个π键,故d错误,
故选:bc.
点评 本题考查有机物的合成与推断、有机反应类型、官能团的结构与性质、限制条件同分异构体的书写等,是对有机化学基础的综合考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | SO2和SiO2 | B. | CO2和H2 | C. | NaCl和HCl | D. | CCl4和KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
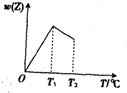 由等物质的量的X气体和Y气体组成的混合气体,在一定条件下进行如图所示的反应:X(g)+Y(g)?nZ(g),经时间t后,产物Z气体在反应混合物中的物质的量百分数与温度的关系如图所示,经分析可知:
由等物质的量的X气体和Y气体组成的混合气体,在一定条件下进行如图所示的反应:X(g)+Y(g)?nZ(g),经时间t后,产物Z气体在反应混合物中的物质的量百分数与温度的关系如图所示,经分析可知:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
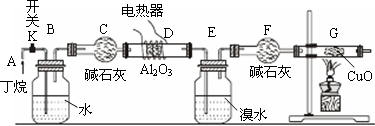
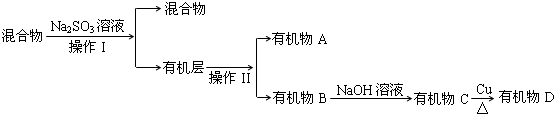
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HOOC-COOH | B. | HO(CH2)2COOH | C. | CH2OHCHOHCOOH | D. | (CH3)3CCOOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [Na+]>[Ac-] | B. | [Na+]>[Ac-] | C. | [Na+]<[Ac-] | D. | [Na+]+[H+]=[OH-]+[Ac-] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时负极反应为:Zn-2e-+2OH-═Zn(OH)2 | |
| B. | 放电时每转移3 mol 电子,正极有1 mol K2FeO4被氧化 | |
| C. | 充电时阳极反应为:Fe(OH)3-3e-+5OH-═FeO${\;}_{4}^{2-}$+4H2O | |
| D. | 充电时阴极附近溶液的碱性增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com