
设NA为阿伏加德罗常数,下列说法错误的是( )
A. 标准状况下22.4LCl2和H2合混气体原子数为2NA
B. lmolNa2O2和足量的水完全反应,转移的电子数为NA
C. 1mol金刚石中含共价键数目为4NA
D. 电解食盐水若产生2g氢气,则转移的电子数目为2NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年江苏省淮安市高一上学期期末调研测试化学试卷(解析版) 题型:实验题
Ⅰ.实验室可以用二氧化锰和浓盐酸反应制取氯气,方程式如下:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,下图是某学生设计的试验室制备干燥Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题:
MnCl2+Cl2↑+2H2O,下图是某学生设计的试验室制备干燥Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题:
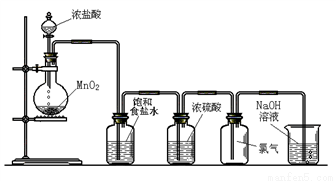
(1)该实验中还缺少一种仪器,这种仪器是_____________;
(2)饱和食盐水的作用是____________________;
(3)氯气与冷的氢氧化钠溶液反应生成NaCl、NaClO和H2O,与热的氢氧化钠溶液按照下面的反应进行:____________________
Cl2+ NaOH(热) - NaCl+ NaClO3+ H2O,请配平上述反应方程式;
(4)8.7 g MnO2和足量的浓盐酸反应,其中被氧化的HCl的物质的量为_________mol。
Ⅱ.某同学为探究铜跟浓硫酸的反应情况,用如图所示装置进行了有关实验。
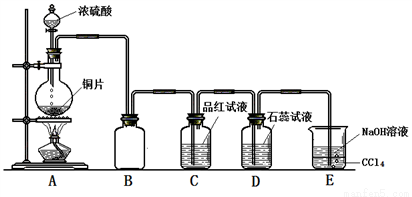
(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请把导管补充完整_____________;
(2)D中的现象是_____________________;
(3)E中NaOH溶液的作用是_________________;
(4)下列药品中能够用来验证反应停止后的烧瓶中有H2SO4剩余的是__________(填字母编号)。
a.BaCl2溶液 b.NaHCO3粉末 c.Ba(NO3)2溶液 d.银粉
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高一上学期期末考试(B卷)化学试卷(解析版) 题型:简答题
完成下列题目
(1)现有以下物质 ① 酒精 ②盐酸 ③熔融KCl ④KOH固体 ⑤蔗糖 ⑥铜 ⑦稀H2SO4溶液
以上物质中属于电解质的是(填序号)________________
(2)同温同压下,同体积的CO2和CO,它们的分子数之比为____________ ,密度之比为_____________。
(3)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒直径的范围是___________________。
(4)下列物质:①Cl2;②Na2CO3;③NaHCO3;④K—Na合金;⑤Na。
广泛用于玻璃、造纸的是______________(填编号,下同)
可用作原子反应堆的导热剂的是________________________。
(5)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
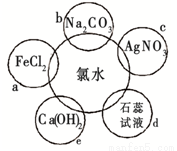
上述反应中发生了氧化还原反应的是:________(填“a”、“b”、“c”或“e”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高一上学期期末考试(B卷)化学试卷(解析版) 题型:选择题
分类法在化学学科发展中起到了非常重要的作用,下列分类标准合理的是( )
A. 根据是否含有氧元素,将物质分为氧化剂和还原剂
B. 根据是否具有丁达尔现象,将分散系分为溶液、胶体和浊液
C. 根据水溶液是否能够导电,将物质分为电解质和非电解质
D. 根据是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三下学期二调考试理综化学试卷(解析版) 题型:选择题
己知某温度下,Ksp(AgCl)=1.56×10-10mol2/L2,Ksp(Ag2CrO4)=1×10-12mol3/L3,下列叙述正确的是( )
A. 饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大
B. 向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小
C. 向0.001mol/L的K2CrO4溶液中加入等体积的0.002mol/L AgNO3溶液,则CrO42-时完全沉淀
D. 将0.00lmol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L K2CrO4溶液,则先产生AgCl沉淀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高一上学期期末考试化学试卷(解析版) 题型:简答题
(1)机智如化学老师的你用固体烧碱配制500mL 0.20 mol L-1的NaOH溶液,需要称取____g固体,定容时除了胶头滴管和玻璃棒,还需要的仪器为______。
(2)语文老师要用36.5% (ρ=1.18g cm-3)的浓盐酸配制0.4 mol L-1的盐酸240 mL,需准确量取36.5%的浓盐酸____mL。
(3)若配制0.5mol L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是_______(填序号)。
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。
B.移液时容量瓶中有少量蒸馏水。
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切。
E.稀释后没冷却到室温就将溶液转移至容量瓶。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高一上学期期末考试化学试卷(解析版) 题型:选择题
把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等,则已反应的Fe3+和未反应Fe3+的物质的量之比为
A. 1:1 B. 1:2 C. 2:3 D. 3:2
查看答案和解析>>
科目:高中化学 来源:广东省2016-2017学年高二上学期期末考试化学(文)试卷 题型:选择题
化学反应速率受很多因素影响。下列措施主要是从降低反应速率的角度考虑的是
A. 将食物置于冰箱中冷藏保存 B. 将FeCl3加入H2O2溶液中制备O2
C. 将洗衣粉溶于温水后洗涤衣服 D. 将CaCO3固体研磨后再与稀HCl反应
查看答案和解析>>
科目:高中化学 来源:广东省2016-2017学年高二上学期期末考试化学(文)试卷 题型:选择题
氢有三种同位素: 、
、 和
和 ,它们之间存在差异的是
,它们之间存在差异的是
A. 中子数 B. 电子数 C. 原子序数 D. 质子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com