
| A.先配制一定量的0.10 mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 |
| B.先测0.10 mol/L CH3COOH溶液的pH,然后将其加热至40℃,再测pH,如果pH变小,则可证明醋酸为弱电解质 |
| C.先配制一定量0.01 mol/L和0.10 mol/L的CH3COOH溶液,分别测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸为弱电解质 |
| D.在常温下,配制一定量的CH3COONa溶液,测其pH,若pH大于7,则可证明醋酸为弱电解质。 |
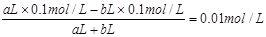 ,解得a:b=11:9。
,解得a:b=11:9。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.物质的量浓度c(甲)=10c(乙) |
| B.甲中H+物质的量浓度是乙的0.1倍 |
| C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)>10V(甲) |
| D.甲中的c(OH-)为乙中c(OH-)的10倍 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3COO- + H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变小的是( )
CH3COO- + H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变小的是( )| A.H2O | B.CH3COONa | C.NH3·H2O | D.H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
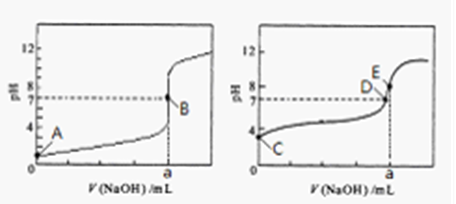
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
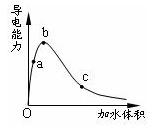
| A.a、b、c三点溶液的pH:c<a<b |
| B.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b |
| C.a、b、c三点中b点n(H+)最大 |
| D.a、b、c三点醋酸的电离程度:a<b<c |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3COO-+H+已达平衡,若要使醋酸的电离平衡向左移动和溶液的pH值都减小,应加入的试剂是
CH3COO-+H+已达平衡,若要使醋酸的电离平衡向左移动和溶液的pH值都减小,应加入的试剂是 | A.CH3COONa | B.NH3·H2O | C.HCl | D.H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解质越弱,则其溶液的导电能力就越差 |
| B.同一弱电解质,浓度越大,电离程度越大 |
| C.升高温度,弱电解质的电离程度减小 |
| D.弱电解质的相对强弱可由相同温度下的电离常数值的大小来判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com