
下列现象与胶体无关的是
A.向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
B.明矾净水
C.将某些胶态金属氧化物分散于玻璃中制成有色玻璃
D.清晨,人们经常看到阳光穿过茂密的树木枝叶所产生的美丽“光柱”
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:2014-2015湖北省荆门市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各组离子可以在溶液中大量共存的是
A.Na+、Ba2+、NO3-、SO42- B.H+、K+、Cl-、OH-
C.K+、H+、NO3-、HCO3- D.K+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:选择题
依据下列热化学方程式得出的结论正确的是
A.已知2H2(g)+O2(g) = 2H2O(g) ΔH=-483.6 kJ· mol-1说明2 mol H2(g)和1 mol O2(g)的能量总和小于2 mol H2O(g)的能量
B.已知C(s,石墨) = C(s,金刚石) ΔH>0,则金刚石比石墨稳定
C.已知NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含20 g NaOH的稀溶液与稀盐酸恰好完全中和,放出28.65 kJ的热量
D.已知2C(s)+2O2(g) = 2CO2(g) ΔH1 ;2C(s)+O2(g) = 2CO(g) ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)霞石是一种硅酸盐,其组成可表示为K2O·3Na2O·4Al2O3·8SiO2,某小组同学设计以霞石为原料制备Al2O3的方案如下:
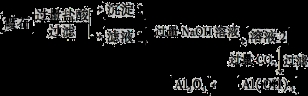
请回答下列问题:
(1)沉淀1的主要成分的化学式为 。
(2)向滤液1中加入过量NaOH溶液的有关反应离子方程式为 。
(3)由溶液2生成Al(OH)3的离子方程式为 。
(4)某同学提出上述流程较繁琐,可简化流程,其方法是向滤液1中加入足量的试剂X即可得到Al(OH)3,则试剂X为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:选择题
在下列物质之间的反应中,水既不是氧化剂又不是还原剂的是
A.F2 + H2O (生成O2和HF) B.Na + H2O
C.NaH + H2O(生成H2和NaOH) D.Na2O2 + H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高一上学期期末考试化学试卷(解析版) 题型:选择题
某物质灼烧时,火焰颜色为黄色,下列判断正确的是
A.该物质是金属钠 B.该物质一定含钠元素
C.该物质是钠的化合物 D.该物质一定含钾元素
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省湛江市高二第一学期期末化学试卷(解析版) 题型:填空题
(11分)(1)FeCl3的水溶液呈____(填“酸”、“中”、“碱”)性,实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以____(填“促进”、“抑制”)其水解。
(2)氯化铝溶于水的反应(用离子方程式表示):_______________________;把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是 。
(3)物质的量浓度均为0.10 mol·L-1的三种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3
pH由小到大排列的顺序是 (用编号填写)。
(4)NaHCO3溶液显 性,原因是_______________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高一上学期期末考试化学试卷(解析版) 题型:选择题
(本小题满分8分)回答下列与氯及其化合物有关的问题
(1)工业上用电解饱和食盐水的方法来制取氯气,请写出反应的化学方程式并用双线桥标出电子转移的方向和数目: 。
(2)人们在日常生活当中常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒。漂白粉的有效成分是(填化学式) 。
某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质有 (填序号)。
A.酸性 B.碱性 C.强氧化性 D.还原性
(3)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3 +4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省龙岩市非一级达标校高二上学期期末化学试卷(解析版) 题型:实验题
(12分)酸碱中和滴定是中学化学中重要的定量实验之一。
Ⅰ.某研究性学习小组准确进行了如下实验,称取1.00g不纯的苛性钠样品配成250ml溶液,取出10.00ml,用已知浓度为0.040mol·L-1的盐酸进行滴定(杂质不与盐酸反应)。
根据要求回答下列问题:
(1)配制250 mL 0.040mol·L-1的盐酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___________和______________。
(2)为测定该苛性钠溶液的准确浓度,几次滴定消耗盐酸的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗盐酸溶液的体积(mL) | 20.05 | 20.00 | 22.10 | 19.95 |
①计算苛性钠浓度时,哪次实验的数据不宜采用?答:________。(填实验序号)
②该苛性钠溶液的浓度为___________。
(3)若操作过程中未用盐酸润洗滴定管,对测定结果有怎样的影响?
答:______________________(填“偏大”、“偏小”或“无影响”)。
Ⅱ.在另一次实验中,研究性小组将V1 mL 1.0mol·L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液均匀混合后,测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。

(4)下列叙述中正确的是_________
A.该实验的环境温度为22℃
B.当V1 =40时,溶液中c(Na+)<c(Cl—)
C.NaOH溶液的浓度为1.0mol·L-1
D.保持其他条件不变,只将HCl改为CH3COOH进行实验,也得到如图的实验结果
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com