
【题目】粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20gA全部溶于0.15L 6.0molL-1盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L(标况)气体。同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检查时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是_________________________________________,产物中的单质是___________。
(2)②中所发生的各反应的化学方程式是_______________________________________。
(3)③中所发生的各反应的离子方程式是 _________________________。
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为 _______________。c(Fe2+)为_____________________。
【答案】加少量KClO3,插上镁条并将其点燃 Fe MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+ 0.67mol/L 2.33mol/L
【解析】
①铝热反应本质是置换反应,金属性Al>Fe,所以发生Al与Fe2O3反应,置换出铁,即B为Fe;
②MgO与盐酸反应生成氯化镁与水,Fe2O3与盐酸反应生成氯化铁与水,溶液C中含有MgCl2、FeCl3;
③单质B和溶液C反应,放出1.12L(标准状况)气体,说明生成氢气,说明②中盐酸过量,溶液C为MgCl2、FeCl3、HCl混合溶液,反应同时生成溶液D,还残留有固体物质B,说明Fe有剩余,结合④用KSCN溶液检验时,溶液D不变色,说明D溶液不含铁离子,则D中溶质为MgCl2、FeCl2。
①铝热反应本质是置换反应,金属性Al>Fe,所以发生Al与Fe2O3反应,置换出铁,即B为Fe;
②MgO与盐酸反应生成氯化镁与水,Fe2O3与盐酸反应生成氯化铁与水,溶液C中含有MgCl2、FeCl3;
③单质B和溶液C反应,放出1.12L(标准状况)气体,说明生成氢气,说明②中盐酸过量,溶液C为MgCl2、FeCl3、HCl混合溶液,反应同时生成溶液D,还残留有固体物质B,说明Fe有剩余,结合④用KSCN溶液检验时,溶液D不变色,说明D溶液不含铁离子,则D中溶质为MgCl2、FeCl2;
(1)①中引发铝热反应操作为:加少量KClO3,插上镁条并将其点燃,产物中的单质B是Fe;
(2)氧化镁与盐酸反应生成氯化镁与水,氧化铁与盐酸反应生成氯化铁与水,反应方程式为:MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O;
(3)Fe与盐酸反应生成氯化亚铁与氢气,反应离子方程式为:Fe+2H+=Fe2++H2↑,铁与氯化铁反应生成氯化亚铁,反应离子方程式为Fe+2Fe3+=3Fe2+;
(4)令MgO和Fe2O3的物质的量分别为xmol,则40x+160x=20,解得x=0.1,溶液D为MgCl2、FeCl2的混合溶液,根据镁元素守恒可知,n(Mg2+)=n(MgO)=0.1mol,所以c(Mg2+)=![]() =0.67mol/L;根据电荷守恒溶液中2c(Mg2+)+2c(Fe2+)=c(Cl﹣),所以2×0.67mol/L+2c(Fe2+)=6mol/L,解得c(Fe2+)=2.33mol/L。
=0.67mol/L;根据电荷守恒溶液中2c(Mg2+)+2c(Fe2+)=c(Cl﹣),所以2×0.67mol/L+2c(Fe2+)=6mol/L,解得c(Fe2+)=2.33mol/L。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】芳香化合物A(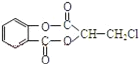 )在一定条件下可以发生如图所示的转化(其他产物和水已略去)。
)在一定条件下可以发生如图所示的转化(其他产物和水已略去)。
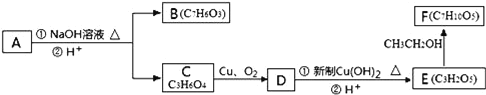
请回答下列问题:
(1)请写出A中包含的官能团的名称:__。
(2)有机物C可以由乳酸经过几步有机反应制得,其中最佳的次序是__。
A.消去、加成、水解、酸化 B.氧化、加成、水解、酸化
C.取代、水解、氧化、酸化 D.消去、加成、水解、氧化
(3)写出由E制得F的化学方程式:__。
(4)1molA在氢氧化钠溶液中加热,充分反应消耗氢氧化钠__mol,写出该反应的化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液阳离子只可能含有:Na+、NH4+、Ba2+、Cu2+、Fe2+、Fe3+、Al3+中的某几种,实验设计了下述方案进行处理,以回收金属,保护环境
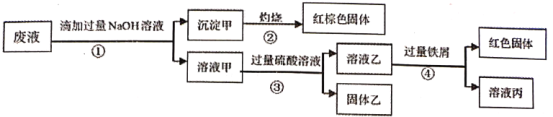
已知:步骤①中,滴加NaOH溶液过程中产生的沉淀会部分溶解,下列说法正确的是:
A.根据步骤①中的现象,说明废液中一定含有Al3+
B.步骤②,由红棕色固体可知,废液中一定存在Fe3+
C.取溶液丙进行焰色反应,焰色为黄色,说明原溶液中一定含Na+
D.该废液一定含有NH4+、Ba2+、Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二氯乙烷是一种广泛使用的有机溶剂、黏合剂,也用作谷物和粮仓的熏蒸剂,沸点83.5℃,熔点-35℃。某研究性学习小组的同学利用如图(加热装置省略)装置制备一定量的1,2-二氯乙烷,制备原理为:C2H5OH![]() C2H4→CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8g/mL 。
C2H4→CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8g/mL 。
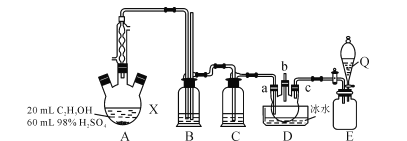
(1)根据制备原理,可知装置A中还缺少的一种实验仪器是________。使用冷凝管的目的是__________________________。
(2)实验时A中三颈烧瓶内有有刺激性气味的无机气体产生,为吸收反应中生成的无机气体,在装置B中应加入________(填字母序号)。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)D中a、c两个导管进入仪器中的长度不同,其优点是________________,对导管b的进一步处理方法是______________________,装置E是氯气的贮气瓶,则Q中的物质是______________。
(4)若得到ag1,2-二氯乙烷,则乙醇的利用率为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电气石是一种具有保健作用的天然石材,其中含有的主要元素为B、Si、Al、Mg、Na、O等元素。
(1)上述元素中,原子半径最小的是_________(用元素符号表示),在元素周期表中处于金属和非金属分界线附近的元素是_____________(用元素符号表示);
(2)表示原子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式,从中选择最详尽描述核外电子运动状态的方式,来表示氧元素原子核外电子的运动状态______________;
(3)B与最活泼的非金属元素F形成化合物BF3,检测发现BF3分子中三根B—F键的键长相等,三根键的键角相等,能否仅仅依据此数据此判断BF3分子的极性____________;
(4)SiO2晶体的熔点比BF3晶体________(选填“高”、“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 甲苯分子中所有原子在同一平面上
B. 苯、乙酸、乙醇均能发生取代反应
C. 分子式为C3H6Cl2的同分异构体共有4种(不考虑立体异构)
D. 可用溴的四氯化碳溶液区别![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I的形式存在,几种粒子之间的转化关系如图所示。已知淀粉遇单质碘变蓝,下列说法中正确的是
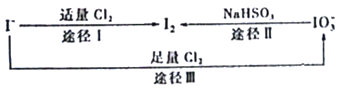
A. 向含I的溶液中通入Cl2,所得溶液加入淀粉溶液一定变蓝
B. 途径II中若生成1 mol I2,消耗1 mol NaHSO3
C. 氧化性的强弱顺序为Cl2>I2>IO3
D. 一定条件下,I与IO3可能生成I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.活泼非金属单质在氧化还原反应中只作氧化剂
C.阳离子只有氧化性,阴离子只有还原性
D.含有某元素最高价态的化合物不一定具有强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为(C7H5NO)。
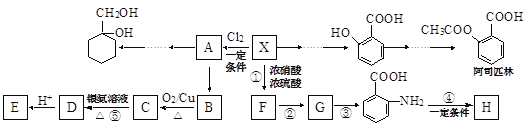
已知:![]() (苯胺,易被氧化)
(苯胺,易被氧化)
完成下列填空:
(1)X的结构简式是______,反应⑤的类型是_________。
(2)反应②③两步能否互换_______(填“能”或“不能”),理由是______。
(3)反应④的化学方程式是____________。
(4)检验B是否完全转化为C的方法是______(选填编号)。
a.定量测熔点 b.定性酸性高锰酸钾溶液
c.定量银氨溶液 d.定性新制氢氧化铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com