
| A. | PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿 | |
| B. | 汽车尾气排放的NO2等气体是造成光化学污染的主要原因 | |
| C. | 点燃爆竹后,硫燃烧生成SO3 | |
| D. | 误食含有大量Cu2+的食物可以服用鲜牛奶解毒 |
分析 A.具有热塑性的塑料具有链状结构,加热熔化、冷却后变成固体,可以反复进行;热固性具有网状结构,一经加工成型就不会受热熔;
B.氮的氧化物会导致酸雨、光化学烟雾;
C.硫燃烧生成SO2;
D.Cu2+是重金属离子,能使蛋白质发生变性.
解答 解:A.PVC属于链状高分子化合物,能溶于氯仿,加热熔化、冷却后变成固体,可以反复进行,故A正确;
B.汽车尾气中含有CO、氮的氧化物,氮的氧化物会导致酸雨、光化学烟雾,故B正确;
C.点燃爆竹后,硫燃烧生成SO2,二氧化硫催化氧化才生成三氧化硫,故C错误;
D.重金属中毒时喝入大量含蛋白质的物质能够有效解毒,鲜牛奶是蛋白质,故D正确.
故选C.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、性质与用途、化学与生活的关系为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气 | |
| B. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 | |
| C. | 滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3. | |
| D. | 钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
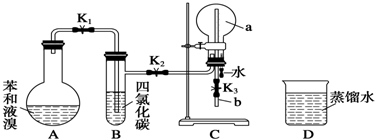
 ,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4、H2O、O2 |
| ② | Cl2、FeBr2 | FeCl3、Br2 |
| ③ | KMnO4、HCl | Cl2、MnCl2 |
| A. | 第①组反应中,H2O2作还原剂 | |
| B. | 第②组反应中,Cl2与FeBr2的物质的量之比可能为3:2 | |
| C. | 第③组反应中,每生成1mol Cl2转移电子2mol | |
| D. | 从三个反应可以得出:氧化性由强到弱顺序为MnO4->Fe3+>Cl2>Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com