
| A. | 锂(Li)与水反应比钠与水反应剧烈 | |
| B. | 砹(At)为有色固体,HAt极不稳定 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | HBrO4的酸性比HIO4的酸性强 |
分析 A.金属的活泼性越强,与水反应的剧烈程度越强;
B.卤族元素,随着原子序数的递增,单质的颜色逐渐加深,生成氢化物的稳定性越弱;
C.金属性越强,与氧气反应生成产物越复杂;
D.非金属性越强,最高价氧化物对应水合物的酸性越强.
解答 解:A.钠的活泼性比锂(Li)强,则与水反应时,钠与水反应更剧烈,故A错误;
B.砹(At)为第七周期、ⅤⅡA族元素,该族元素单质的颜色逐渐加深,对于氢化物稳定性逐渐减弱,则砹为有色固体,且HAt极不稳定,故B正确;
C.铷的金属性大于钠,则在氧气中铷(Rb)的燃烧产物比钠的燃烧产物更复杂,故C正确;
D.非金属性:Br>I,则最高价氧化物对应水合物酸性:HBrO4的酸性比HIO4的酸性,故D正确;
故选A.
点评 本题考查了元素周期律内容及其应用,题目难度中等,明确元素周期律内容为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | CH2=CH(CH2)2CH3 | B. | CH2=CH(CH2)3CH3 | ||
| C. | CH3CH=CHCH=CHCH3 | D. | CH3CH2CH=CHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60与金刚石一样属于原子晶体 | |
| B. | 水结冰体积膨胀、密度变小,这一事实与水分子间存在氢键有关 | |
| C. | 分子晶体中必含化学键 | |
| D. | 干冰升华破坏了共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol | B. | 0.05mol | C. | 0.15mol | D. | 0.11mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | ⅥⅠA族元素的氢化物中,稳定性最好的沸点也最高 | |
| C. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| D. | 同周期非金属元素氧化物对应水化物的酸性从左到右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验内容 | 实验目的 |
| A | 在碘水中加入约1mL四氯化碳,振荡试管,观察碘被四氯化碳萃取,再向试管里加入1mL浓KI水溶液,振荡试管,溶液紫色变浅 | 证明物质的溶解性规律--“相似相溶” |
| B | 取两只试管,分别加入4mL0.01mol/L KMnO4酸性溶液,然后向一只试管中加入0.1mol/LH2C2O4溶液2mL,向另一只试管中加入0.1mol/LH2C2O4溶液4mL,记录褪色时间 | 证明草酸浓度越大反应速率越快 |
| C | 分别向2mL甲苯、2mL苯、2mL正己烷中加入3滴酸性高锰酸钾溶液,振荡.甲苯中酸性高锰酸钾溶液褪色,而苯、正己烷中酸性高锰酸钾溶液不褪色 | 证明与苯环相连的甲基易被氧化 |
| D | 将反应产生的气体依次通入盛有NaOH溶液、品红溶液及酸性KMnO4溶液的试管,品红不褪色,酸性KMnO4溶液褪色 | 证明乙醇与浓硫酸混合加热可得乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
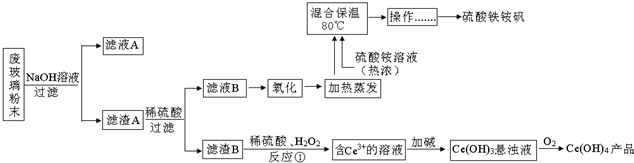

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com