
| A. | ①③④ | B. | ①②④ | C. | ①②③④ | D. | ①②④⑤ |
分析 若要加快产生氢气的速率,可增大反应的浓度、增大固体的表面积、升高温度以及形成原电池反应,注意加入浓硫酸的性质,以此解答该题.
解答 解:①适当升高温度,增大活化分子百分数,反应速率加快,故正确;
②改用100mL 1.0mol/LH2SO4溶酸,酸的浓度增大,反应速率加快,故正确;
③改用300mL 0.5mol/LH2SO4溶液,酸的浓度不变,反应速率不变,故错误;
④用等量铁粉代替铁片,增大固体接触面积,使反应速率加快,故正确;
⑤改用300mL18.0mol/LH2SO4溶液,浓硫酸与铁不生成氢气,则不能加快反应速率,故错误;
综上所述,①②④正确;
故选B.
点评 本题考查化学反应速率的影响因素,为高频考点,把握接触面积、温度、浓度等对反应速率的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SO4>H2CO3 | B. | 沸点:CBr4>CCl4 | ||
| C. | 碱性:Al(OH)3>NaOH | D. | 热稳定性:HF>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 滤液为NaCl饱和溶液 | B. | 滤液中NaCl的质量分数为36% | ||
| C. | 该温度下,NaCl的溶解度为50g | D. | 该温度下,NaCl的溶解度为36g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据周期元素的原子半径变化趋势,推出Al的半径比Mg大 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据同主族元素化学性质相似规律,推出Li在空气中完全燃烧的产物是Li2O2 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入Na2SiO3溶液中能生成H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径Na>Mg>Al | |
| B. | 碱性NaOH>Mg(OH)2>Al (OH)3 | |
| C. | 阳离子的氧化性Na+<Mg2+<Al3+ | |
| D. | Na与冷水剧烈反应,Mg与冷水反应微弱;镁粉与铝粉分别与同浓度稀HCl反应,镁粉比铝粉反应剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的热稳定性:Y>Z | |
| B. | W与另外三种元素均可形成离子键 | |
| C. | 简单离子半径:W>Y>Z | |
| D. | W和Y可形成阴阳离子个数比是1:1的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该物质的结构简式为 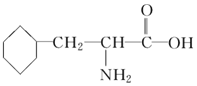 | |
| B. | 该物质可以发生加成反应 | |
| C. | 该物质既可以与强酸反应,但不可以与强碱反应 | |
| D. | 该物质不可以聚合成高分子物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com