
| KI溶液(I2) | MnO2固体 (Fe) | 氯气(氯化氢) | NaCl溶液 (NaBr) | KI固体 (I2) | |
| 加入试剂 | 此处不填 | ||||
| 分离方法 |
分析 碘易溶于有机溶剂,可用萃取分液的方法分离;铁可与稀盐酸反应,而二氧化锰与稀盐酸不反应;氯气不溶于饱和食盐水;氯气可与NaBr反应生成NaCl和溴,碘易升华,可加热分离,以此解答该题.
解答 解:碘易溶于有机溶剂,可加入四氯化碳用萃取分液的方法分离;
铁可与稀盐酸反应,而二氧化锰与稀盐酸不反应,可加入盐酸,然后过滤分离;
氯气不溶于饱和食盐水,可用洗气装置分离;
氯气可与NaBr反应生成NaCl和溴,可加新制Cl2水/CCl4,然后分液;
碘易升华,可加热分离,
故答案为:
| KI溶液(I2) | MnO2固体 (Fe) | 氯气(氯化氢) | NaCl溶液 (NaBr) | KI固体 (I2) | |
| 加入试剂 | 2 | 3 | 1 | 4 | 此处不填 |
| 分离方法 | C | D | B | C | A |
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的化学反应、混合物分离提纯方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 除去杂质使用的试剂 | 除去杂质的方法 |
| A | CO2气体(HC1气) | 饱和Na2CO3溶液,浓硫酸 | 洗气 |
| B | NH4Cl固体(I2) | 加热 | |
| C | FeCl2溶液(FeCl3) | 氯水 | |
| D | MgCl2溶液(A1C13) | NaOH溶液,稀盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 铁粉溶于浓盐酸:Fe+2H+=Fe2++H2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| D. | 小苏打溶液中加入盐酸:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
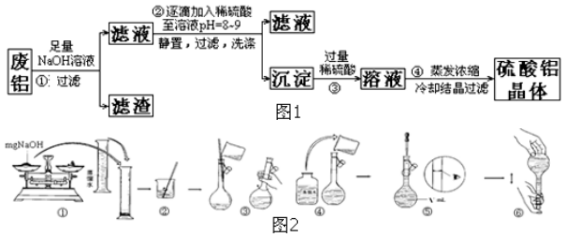
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 4:1 | C. | 1:4 | D. | 8:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于N2分子中的N≡N键能大,因此其沸点高于CH4 | |
| B. | 固体CH4中的化学键只有极性共价键 | |
| C. | 冥王星表面可能不会有大量O2存在 | |
| D. | CH4可以作燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用HF溶液做导电性实验,灯泡很暗 | |
| B. | HF与水能以任意比混溶 | |
| C. | 1mol/L的HF水溶液能使紫色石蕊试液变红 | |
| D. | 常温下NaF溶液的pH大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ①④⑥ | D. | ⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com