
【题目】氮、硫、碳的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:
(1)根据A对应的化合价和物质类别,A为___________(写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有____________。
(2)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________,反应的离子方程式为______________。
(3)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题:

①写出制取SO2的化学方程式:_______________。
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为_____。
A. 品红溶液 B. 酸性高锰酸钾溶液 C. 双氧水(H2O2)
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学反应方程式_______。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2吸收Br2反应的化学方程式为____________。
【答案】N2O5 NO、NO2 浓硝酸 Cu+4H++2NO3-=Cu2++2NO2↑+2H2O Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O B NO+NO2+2NaOH=2NaNO2+H2O SO2+Br2+2H2O=H2SO4+2HBr
CuSO4+SO2↑+2H2O B NO+NO2+2NaOH=2NaNO2+H2O SO2+Br2+2H2O=H2SO4+2HBr
【解析】
(1)依据图中化合价与元素化合物之间关系可知A为+5价氧化物;所含元素化合价处于中间价态的既有氧化性又有还原性;
(2)铜与浓硝酸反应生成硝酸铜、二氧化氮和水,铁与浓硝酸常温下发生钝化;
(3)①铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水;
②依据二氧化硫能使酸性高锰酸钾溶液褪色检验二氧化硫的还原性;
(4)NaOH与NO、NO2会发生归中反应产生NaNO2H2O,据此书写反应方程式;
(5)二氧化硫与溴水反应生成溴化氢和硫酸。
(1)依据图中化合价与元素化合物之间关系可知A为+5价的氮元素的氧化物,为N2O5;N原子最外层有5个电子,最高为+5价,最低为-3价,NO、NO2中氮元素处于中间价态,化合价既可以升高,又可以降低,所以NO、NO2既有氧化性又有还原性;
(2)铜与浓硝酸反应生成硝酸铜、NO2和水,铁与浓硝酸在常温下会发生钝化,所以可用浓硝酸除去铁制品表面的铜镀层,反应的离子方程式:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(3)①在实验室中,一般是用铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,化学方程式:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
②二氧化硫的具有还原性,能够使酸性KMnO4溶液紫色褪色,所以检验SO2的还原性可选酸性高锰酸钾溶液,故合理选项是B;
(4)NO、NO2是大气污染物,可用NaOH溶液进行尾气处理,反应的化学方程式为:NO+NO2+2NaOH=2NaNO2+H2O;
(5)二氧化硫与溴水反应生成溴化氢和硫酸,化学方程式:SO2+Br2+2H2O=H2SO4+2HBr。


科目:高中化学 来源: 题型:
【题目】向体积均为2 L的两个恒容密闭容器中分别充入1molSiHCl3,维持容器的温度分别为T1℃和T2℃不变,发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
SiH2Cl2(g)+SiCl4(g) ΔH1=a kJ·mol1。反应过程中SiHCl3的转化率随时间的变化如图所示。下列说法正确的是
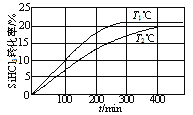
A.T1>T2
B.T1℃时,0~100min反应的平均速率v(SiHCl3)=0.001mol·(L·min)-1
C.T2℃时,反应的平衡常数:K=1/64
D.T2℃时,使用合适的催化剂,可使SiHCl3的平衡转化率与T1℃时相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
① C2H2(g) +![]() O2(g) = 2CO2(g)+H2O(l) ΔH1=-1301.0 kJmol-1
O2(g) = 2CO2(g)+H2O(l) ΔH1=-1301.0 kJmol-1
② C(s)+ O2(g) = CO2(g) △H2=-393.5 kJmol-1
③ H2(g)+![]() O2(g) = H2O(l) △H3 = -285.8 kJ·mol-1
O2(g) = H2O(l) △H3 = -285.8 kJ·mol-1
则反应④ 2C(s)+ H2(g) = C2H2(g)的△H为( )
A.+228.2 kJ·mol-1B.-228.2 kJ·mol-1
C.+1301.0 kJ·mol-1D.+621.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。
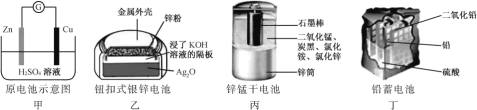
下列说法不正确的是( )
A. 甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B. 乙:正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C. 丙:锌筒作负极,发生氧化反应,锌筒会变薄
D. 丁:电池放电过程中,硫酸浓度不断减少。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应:A(s)+3B(g) ![]() 2C(g)+D(g) 已达平衡状态的是
2C(g)+D(g) 已达平衡状态的是
A.混合气体的压强B.混合气体的密度
C.B和C的物质的量浓度相等D.气体的总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节日期间因燃放鞭炮会引起空气中SO2含量增高,造成大气污染。某实验小组同学欲探究SO2的性质,并测定空气中SO2的含量。
(1)他们设计如图实验装置,请你参与探究,并回答问题:
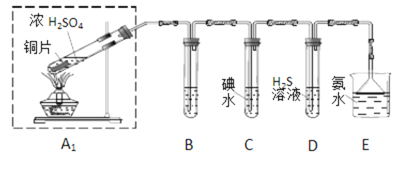
①装置B用于检验SO2的漂白性,其中所盛试剂为______,装置D用于检验SO2的________性质,该装置中反应的化学方程式为_________________________;
②为了实现绿色环保的目标,甲同学欲用装置A2代替装置A1,你认为装置A2的优点是(写两点)_____________、____________;
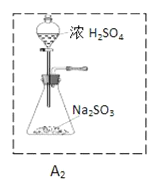
(2)他们拟用以下方法测定空气中SO2含量(假设空气中无其他还原性气体)。

①你认为哪个装置可行(填序号)_______,使用你所选用的装置测定SO2含量时,还需要测定的物理量是__________________;
②你认为哪个装置不可行(填序号)____,说明理由_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质中是同系物的有________;互为同分异构体的有____________;互为同素异形体的有________;互为同位素的有________;
(1)液氯(2)氯气(3)白磷(4)红磷(5)D(6)T(7)![]() (8)
(8)![]() (9)CH2=CH-CH3 (10)
(9)CH2=CH-CH3 (10)![]() (11)2,2—二甲基丁烷
(11)2,2—二甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定是分析化学中最要的分析方法之一,根据其原理回答下列问题:
I、酸碱中和滴定是最基本的滴定方法:
(1)滴定管是酸碱中和滴定中重要的仪器,向25mL碱式滴定管中加入氢氧化钠溶液,开始时滴定管的读数为10.00mL,将滴定管中的液体全部放出,放出氢氧化钠溶液的体积为____________(填“大于”、“小于”或“等于”)15.00mL。
(2)向碱式滴定管中注入标准的氢氧化钠溶液之前的一步操作为(_______________)
(3)准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.1000 mol/LNaOH溶液滴定。下列说法正确的是(______)
A.锥形瓶用蒸馏水洗涤后,用待测HCl溶液润洗
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏大
II、氧化还原滴定也是分析化学中常用的分析手段,用氧化还原滴定方法测定粗品中Na2S2O35H2O的质量分数。
实验步骤:称取6g粗品配制250mL的溶液待用。用酸式滴定管取25.00mL0.01mol/L K2Cr2O7溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的Na2S2O3溶液滴定至终点(反应为I2+2S2O32-=2I﹣+S4O62﹣),消耗Na2S2O3溶液25.00mL。回答下列问题:
(1)向K2Cr2O7溶液中加入过量的KI溶液并酸化,Cr2O72-被还原成Cr3+,写出该反应的离子方程式_____。
(2)用Na2S2O3溶液滴定至终点的现象为_________________________。
(3)粗品中Na2S2O35H2O的质量分数为___________________。
(4)若在取K2Cr2O7溶液时有部分溶液滴到了锥形瓶外,则测定结果偏_________(填“高”、“低”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品工业和食品工业。下图是乙酸苯甲酯的一种合成路线![]() 部分反应物、产物和反应条件略去
部分反应物、产物和反应条件略去![]()

![]() 反应
反应![]() 的类型是________________。
的类型是________________。
![]() 反应
反应![]() 的化学方程式为_____________________________。
的化学方程式为_____________________________。
![]() 的化学方程式为_______________________________。
的化学方程式为_______________________________。
![]() 与E互为同分异构体的芳香族化合物有________种,其中一种同分异构体的核磁共振氢谱有三种类型氢原子的吸收峰,该同分异构体的结构简式为_________________。
与E互为同分异构体的芳香族化合物有________种,其中一种同分异构体的核磁共振氢谱有三种类型氢原子的吸收峰,该同分异构体的结构简式为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com