
【题目】无色的混合气体甲,可能含NO、CO2、NO2、N2中的几种,将一定量的甲气体经过如图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )

A.NO2、N2B.NO、CO2
C.NO2、CO2D.NO、CO2、N2
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】从废旧锂离子二次电池(主要成分为![]() ,还含有少量石墨和金属钢売、铝箔等杂质)中回收钴和锂的工艺流程如下:回答下列问题:
,还含有少量石墨和金属钢売、铝箔等杂质)中回收钴和锂的工艺流程如下:回答下列问题:

(1)![]() 的电子式为__________。“碱浸”的目的是____________。
的电子式为__________。“碱浸”的目的是____________。
(2)“酸浸”过程中![]() 发生反应的离子方程式为______________,浸渣中含有的主要成分是_______________________。
发生反应的离子方程式为______________,浸渣中含有的主要成分是_______________________。
(3)“萃取净化”除去的杂质离子除![]() 外,还有________(填离子符号)
外,还有________(填离子符号)
(4)“苯取分离“中钴、锂的萃取率与平衡时溶液![]() 的关系如图所示,
的关系如图所示,![]() 一般选择5左右,理由是_____________________________________。
一般选择5左右,理由是_____________________________________。

(5)“沉锂“中![]() 的溶解度随温度变化的曲线如图所示:
的溶解度随温度变化的曲线如图所示:
①根据平衡原理分析![]() 在水中的溶解度随温度变化的原因______________。
在水中的溶解度随温度变化的原因______________。
②为获得高纯![]() ,提纯操作依次为热过滤、_______、烘干。
,提纯操作依次为热过滤、_______、烘干。
③若“沉锂”中![]() ,加入等体积等浓度
,加入等体积等浓度![]() 溶液,则此时沉锂率为________________。(已知
溶液,则此时沉锂率为________________。(已知![]() 的
的![]() 为
为![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
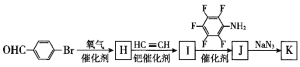
【题目】“点击化学”是指快速、高效连接分子的一类反应,例如铜催化的Huisgen环加成反应:

我国科研人员利用该反应设计、合成了具有特殊结构的聚合物F并研究其水解反应。合成线路如下图所示:

已知:
![]()
(1)①的反应类型是___________,化合物  的官能团的名称为_____________。
的官能团的名称为_____________。
(2)关于B和C,下列说法不正确的是____________(填字母序号)。
a.利用红外光谱法可以鉴别B和C b.B可以发生氧化、取代、消去反应
c.可用溴水检验C中含有碳碳三键
(3)B生成C的过程中还有另一种生成物X,分子式为C3H6O,核磁共振氢谱显示只有一组峰,X的结构简式为______________________。
(4)D生成E的化学方程式为___________________________________________________。
(5)有机物M是有机物C的同系物,其相对分子质量比C大14,写出一种满足下列条件的M的同分异构体N的结构简式是________________________。
a.除苯环外,不含其它的环状结构,不考虑立体异构;
b.能与FeC13溶液发生显色反应;
c.1mol N最多与6mol Br2(浓溴水)反应。
(6)为了探究连接基团对聚合反应的影响,设计了单体K( ) 其合成路线如下,写出H、J的结构简式:H____________、J_______________。
) 其合成路线如下,写出H、J的结构简式:H____________、J_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示,下列说法正确的是
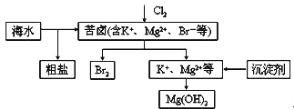
A. 得到的 Mg(0H)2 是耐火砖的主要成分
B. 粗盐可采用除杂和蒸馏等过程提纯
C. 工业生产中常选用 NaOH 作为沉淀剂
D. 富集溴一般先用空气或水蒸气吹出单质溴,再用碱液或SO2 等吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(7分)实验室用加热固体氯化铵和氢氧化钙的混合物制取氨,反应的化学方程式为: 。
所制得气体中常含有少量杂质气体,为了得到纯净的氨气并加以检验,请在下列装置或试剂中,根据要求作出适当选择,并将编号字母填入表中的空格处。
(1)装置:

(2)试剂: a.NaOH溶液 b.澄清石灰水 c.浓硫酸 d.饱和NaHCO3溶液
e.碱石灰 f.品红溶液 g.湿润的红色石蕊试纸
制取气体 | 杂质气体 | 制取气体的发生装置 | 除去杂质气体的净化装置 | 收集装置 | 净化装置内 所用试剂 | 检验制得气体所用试剂 |
NH3 | H2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ实验室里需要纯净的氯化钠溶液,但实验室只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案进行提纯:

(1)操作②能否改为加硝酸钡溶液,______(填“能”或“否”) ,理由_____________________________。
(2)进行操作②后,如何判断SO42- 已除尽,方法是___________________。
(3)操作④的目的是_______________________________。
Ⅱ硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3mol/L H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1中,分离操作,所用到的玻璃仪器有___________________________。(填仪器编号)
①漏斗 ②分液漏斗 ③烧杯 ④广口瓶 ⑤铁架台 ⑥玻璃棒 ⑦酒精灯
(2)在步骤3中,“一系列操作”依次为_____________________、_______________________和过滤。
(3)实验室欲用18mol/L H2SO4来配制240mL 3mol/L H2SO4溶液,需要量取________mL浓硫酸,实验时,下列操作会造成所配溶液浓度偏低的是__________________。(填字母)
a.容量瓶内壁附有水珠而未干燥处理 b.未冷却至室温直接转移至容量瓶中
c.加水时超过刻度线后又倒出 d.定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素存在于黑香豆、香蛇鞭菊、野香荚兰、兰花中,具有新鲜干草香和香豆香,是一种口服抗凝药物。实验室合成香豆素的反应和实验装置如下:

可能用到的有关性质如下:
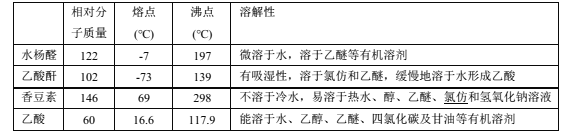
合成反应:
向三颈烧瓶中加入95%的水杨醛38.5g、新蒸过的乙酸酐73g和1g无水乙酸 钾,然后加热升温,三颈烧瓶内温度控制在145~150℃,控制好蒸汽温度。此时,乙酸开始蒸出。当蒸出量约15g时,开始滴加15g乙酸酐,其滴加速度应与乙酸蒸出的速度相当。乙酸酐滴加完毕后,隔一定时间,发现气温不易控制在120℃时,可继续提高内温至208℃左右,并维持15min至半小时,然后自然冷却。
分离提纯:
当温度冷却至80℃左右时,在搅拌下用热水洗涤,静置分出水层,油层用10%的 碳酸钠溶液进行中和,呈微碱性,再用热水洗涤至中性,除去水层,将油层进行减压蒸馏,收集150~160℃/1866Pa馏分为粗产物。将粗产物用95%乙醇(乙醇与粗产物的质量比为1:1)进行重结晶,得到香豆素纯品35.0g。
(1)装置a的名称是_________。
(2)乙酸酐过量的目的是___________。
(3)分水器的作用是________。
(4)使用油浴加热的优点是________。
(5)合成反应中,蒸汽温度的最佳范围是_____(填正确答案标号)。
a.100~110℃ b.117.9~127.9℃ c.139~149℃
(6)判断反应基本完全的现象是___________。
(7)油层用10%的碳酸钠溶液进行中和时主要反应的离子方程式为______。
(8)减压蒸馏时,应该选用下图中的冷凝管是_____(填正确答案标号)。
a.直形冷凝管 b.球形冷凝管
b.球形冷凝管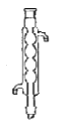 c.蛇形冷凝管
c.蛇形冷凝管
(9)本实验所得到的香豆素产率是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素剧期表的一部分,请根据要求填空

(1) 元素②最外层有_____个电子,在化合物中的最低负化合价为________;
(2) 元素⑤形成的离子的结构汞意图为_________;
(3) 用电子式表示元素①和⑦组成的化合物的形成过程:_______________;
(4) 元素④、⑤的最高价氧化物的水化物之间发生反应的离子方程式______________ 。
(5) 下列选项中能证明元素⑦的非金属性强于元素⑥的是________(双选)。
A.H2S的酸性弱于HCl B.S2-的还原性强于C1-
C.H2SO3的酸性强于HClO D.H2S不如HC1稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下物质:①NaHSO4晶体,②液态O2 ,③冰醋酸(固态醋酸), ④汞,⑤BaSO4固体,⑥Fe(OH)3 胶体,⑦酒精(C2H5OH) ,⑧熔化KNO3,⑨盐酸,⑩金属钠,请回答下列问题(用序号):
(1)以上物质中能导电的是__________
(2)以上物质属于电解质的是_____________
(3)以上物质中属于非电解质的是_______
(4)请写出①在熔融状态下的电离方程式________________
(5)a. 写出制备⑥的实验操作为_________;
b. 制备⑥的离子方程式为____________________,
c. 在制得的⑥中逐滴加入稀硫酸的实验现象为_____________________________。
(6)写出⑩在加热条件下与氧气反应的化学方程式________________________。若将2.3克钠放入97.7克水中,生成的溶液中溶质的质量分数_________(填“大于”、“小于” 或“等于”)2.3%。
(7)标准状况下,CO与CO2相对于②的密度为1,则混合气体中CO与CO2的比例为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com