
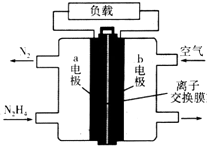
 液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.下列关于该电池的叙述不正确的是( )
液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.下列关于该电池的叙述不正确的是( )| A. | a极的反应式:N2H4+4OH--4e-═N2↑+4H2O | |
| B. | 放电时,电子从a极经过负载流向b极 | |
| C. | 该电池持续放电时,离子交换膜需选用阴离子交换膜 | |
| D. | 电路中转移电子3NA时消耗氧气16.8 L |
分析 该燃料电池中,负极上燃料失电子发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,正极上氧气得电子发生还原反应,电极反应式为:O2+2H2O+4e-=4OH-,电池总反应为:N2H4+O2=N2↑+2H2O,结合离子的移动方向、电流的方向分析解答.
解答 解:A.通入燃料的电极为负极,负极上燃料失电子发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,故A正确;
B.放电时,电流从正极b经过负载流向a极,电子从a极经过负载流向b极,故B正确;
C.该原电池中,正极上生成氢氧根离子,所以离子交换膜要选取阴离子交换膜,故C正确;
D.该电池的总反应为:N2H4+O2=N2↑+2H2O,转移8mol电子,需要1mol氧气,那么转移3mol电子,需要氧气标况下的体积为:$\frac{3}{8}×22.4$L=8.4L,故D错误,故选D.
点评 本题考查了燃料电池,明确正负极上发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质溶液的酸碱性书写,注意电流的方向和电子的流向相反,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 编号 | A | B | C | D |
| 实验 方案 | 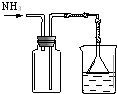 |  | 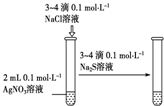 |  置于光亮处 |
| 实验 目的 | 收集氨气及并进行 尾气吸收 | 制取乙炔并验证炔烃 的性质 | 验证AgCl沉淀可转化为 溶解度更小的Ag2S沉淀 | 验证甲烷与氯气发生化学反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 原子序数 | 元素 | 有关信息 |
 | W | 质子数与Y的最外层电子数相等 |
| X | 最低化合价为-2 | |
| Y | 四种元素种仅有的金属元素 | |
| Z | 与Y的原子序数之和为W、X原子序数之和的3倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定前,盐酸和醋酸溶液中:c(Cl?)<c(CH3COO-) | |
| B. | 分别加入10.00 mL NaOH溶液时,测得醋酸反应后所得溶液pH=6,则溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$>1 | |
| C. | 当两种溶液的pH均等于7时,两种酸所消耗NaOH溶液体积不相等,醋酸消耗的NaOH溶液体积多 | |
| D. | 加入20.00 mL NaOH溶液时,所得两种溶液中:c(Cl?)<c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅太阳能电池板在工作时,可以将化学能转化为电能 | |
| B. | 用纯碱溶液可洗涤餐具上的油污 | |
| C. | 用灼烧并闻气味的方法可区别真丝织物和人造棉 | |
| D. | 水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 分子式为C4H6O3,每摩尔该物质充分燃烧需消耗4mol O2 | |
| B. | 能发生取代、加成、氧化、加聚、中和等反应 | |
| C. | 分别与足量Na、NaOH、Na2CO3反应,生成物均为NaOOC-CH═CH-CH2OH | |
| D. | 该分子含有两种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电解饱和食盐水可制得金属钠 | B. | 海带提碘只涉及物理变化 | ||
| C. | 海水提溴涉及到氧化还原反应 | D. | 海水提镁涉及到复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com