
ЁОЬтФПЁП6-ЯѕЛљКњНЗЛљЫсKЪЧКЯГЩаФбЊЙмРрвЉЮяУзТчЩГаЧЕФжаМфЬхЃЌдкЪЕбщЪвжаКЯГЩТЗЯпШчЯТЭМЫљЪО(ВПЗжЗДгІЬѕМўвбОТдШЅ):
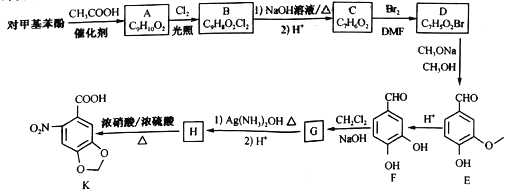
вбжЊ:СЌдкЭЌвЛИіЬМЩЯЕФСНИієЧЛљвзЭбЫЎаЮГЩєЪЛљЁЃ
ЛиД№ЯТСаЮЪЬт:
(1)CЕФУћГЦЮЊ_______ЃЌH жаЙйФмЭХЕФУћГЦЮЊ__________ЁЃ
(2)гЩCЩњГЩDЕФЗДгІРраЭЮЊ_______ЃЌG ЕФНсЙЙМђЪНЮЊ_______ ЁЃ
(3)гЩAЩњГЩBЕФЛЏбЇЗНГЬЪНЮЊ_______ ЁЃ
(4)RЪЧEЕФЭЌЗжвьЙЙЬхЃЌRжагаСНИіШЁДњЛљЃЌЦфжавЛИіЮЊєЧЛљЧвгыБНЛЗжБНгЯрСЌЃЌСэвЛИіШЁДњЛљКЌгаЁА![]() ЁБЃЌЗћКЯЬѕМўЕФRга_____жжЁЃЦфжаКЫДХЙВеёЧтЦзЯдЪОга5жжВЛЭЌРраЭЕФЧтЃЌЧвЗхЕФУцЛ§жЎБШЮЊ2 :2 :2: l: 1ЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНЮЊ________ЁЃ
ЁБЃЌЗћКЯЬѕМўЕФRга_____жжЁЃЦфжаКЫДХЙВеёЧтЦзЯдЪОга5жжВЛЭЌРраЭЕФЧтЃЌЧвЗхЕФУцЛ§жЎБШЮЊ2 :2 :2: l: 1ЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНЮЊ________ЁЃ
(5)аДГівдСкБНЖўЗг![]() КЭввДМЮЊдСЯжЦБИ
КЭввДМЮЊдСЯжЦБИ![]() ЕФКЯГЩТЗЯп____________(ЦфЫћЮоЛњЪдМСШЮбЁ)ЁЃ
ЕФКЯГЩТЗЯп____________(ЦфЫћЮоЛњЪдМСШЮбЁ)ЁЃ
ЁОД№АИЁП ЖдєЧЛљБНМзШЉ єШЛљЁЂУбМќ ШЁДњЗДгІ 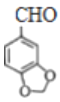
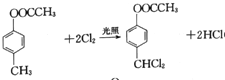 12
12 ![]() ЁЂ
ЁЂ![]()
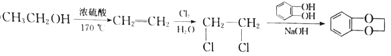
ЁОНтЮіЁПИљОнСїГЬЭМЃЌЖдМзЛљБНЗггыввЫсЗЂЩњѕЅЛЏЗДгІЩњГЩAЃЌAЮЊ ![]() ЃЌ
ЃЌ![]() гыТШЦјдкЙтееЬѕМўЯТЗЂЩњБНЛЗВрСДЕФШЁДњЗДгІЃЌBЮЊ
гыТШЦјдкЙтееЬѕМўЯТЗЂЩњБНЛЗВрСДЕФШЁДњЗДгІЃЌBЮЊ![]() ЃЌСЌдкЭЌвЛИіЬМЩЯЕФСНИієЧЛљвзЭбЫЎаЮГЩєЪЛљЃЌBдкЧтбѕЛЏФЦШмвКжаЫЎНтЩњГЩCЃЌCЮЊ
ЃЌСЌдкЭЌвЛИіЬМЩЯЕФСНИієЧЛљвзЭбЫЎаЮГЩєЪЛљЃЌBдкЧтбѕЛЏФЦШмвКжаЫЎНтЩњГЩCЃЌCЮЊ![]() ЃЌCгыфхЗЂЩњБНЛЗЩЯЕФШЁДњЗДгІЩњГЩDЃЌDЮЊ
ЃЌCгыфхЗЂЩњБНЛЗЩЯЕФШЁДњЗДгІЩњГЩDЃЌDЮЊ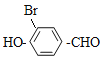 ЃЛИљОнСїГЬЭМЃЌGФмЙЛЗЂЩњвјОЕЗДгІЃЌЫЕУїGжаКЌгаШЉЛљЃЌдђGЮЊ
ЃЛИљОнСїГЬЭМЃЌGФмЙЛЗЂЩњвјОЕЗДгІЃЌЫЕУїGжаКЌгаШЉЛљЃЌдђGЮЊ![]() ЃЌHЮЊ
ЃЌHЮЊ![]() ЁЃ
ЁЃ
(1)ИљОнЩЯЪіЗжЮіЃЌCЮЊ![]() ЃЌУћГЦЮЊЖдєЧЛљБНМзШЉЃЌHЮЊ
ЃЌУћГЦЮЊЖдєЧЛљБНМзШЉЃЌHЮЊ![]() ЃЌЦфжаЕФЙйФмЭХгаєШЛљЁЂУбМќЃЌЙЪД№АИЮЊЃКЖдєЧЛљБНМзШЉЃЛ єШЛљЁЂУбМќЃЛ
ЃЌЦфжаЕФЙйФмЭХгаєШЛљЁЂУбМќЃЌЙЪД№АИЮЊЃКЖдєЧЛљБНМзШЉЃЛ єШЛљЁЂУбМќЃЛ
(2)гЩCЃЈ![]() ЃЉЩњГЩDЃЈ
ЃЉЩњГЩDЃЈ ЃЉЗЂЩњЕФЪЧБНЛЗЕФШЁДњЗДгІЃЌGЕФНсЙЙМђЪНЮЊ
ЃЉЗЂЩњЕФЪЧБНЛЗЕФШЁДњЗДгІЃЌGЕФНсЙЙМђЪНЮЊ![]() ЃЌЙЪД№АИЮЊЃКШЁДњЗДгІЃЛ
ЃЌЙЪД№АИЮЊЃКШЁДњЗДгІЃЛ![]() ЃЛ
ЃЛ
(3)ИљОнЩЯЪіЗжЮіЃЌгЩAЩњГЩBЕФЛЏбЇЗНГЬЪНЮЊ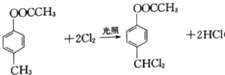 ЃЌЙЪД№АИЮЊЃК
ЃЌЙЪД№АИЮЊЃК ЃЛ
ЃЛ
(4)RЪЧEЃЈ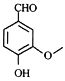 ЃЉЕФЭЌЗжвьЙЙЬхЃЌRжагаСНИіШЁДњЛљЃЌЦфжавЛИіЮЊєЧЛљЧвгыБНЛЗжБНгЯрСЌЃЌСэвЛИіШЁДњЛљЕФЛЏбЇЪНЮЊЁЊC2H3O2ЃЌвђЮЊСэвЛИіШЁДњЛљКЌгаЁА
ЃЉЕФЭЌЗжвьЙЙЬхЃЌRжагаСНИіШЁДњЛљЃЌЦфжавЛИіЮЊєЧЛљЧвгыБНЛЗжБНгЯрСЌЃЌСэвЛИіШЁДњЛљЕФЛЏбЇЪНЮЊЁЊC2H3O2ЃЌвђЮЊСэвЛИіШЁДњЛљКЌгаЁА![]() ЁБЃЌЗћКЯЬѕМўЕФЁЊC2H3O2гаЁЊCOOCH3ЁЂЁЊCH2COOHЁЂЁЊCH2OOCHЁЂЁЊOOCCH3ЃЌБНЛЗЩЯЕФЖўИіШЁДњЛљгаСкЁЂМфЁЂЖд3жжЮЛжУЙиЯЕЃЌвђДЫRЕФЭЌЗжвьЙЙЬхга3ЁС4=12жжЃЌЦфжаКЫДХЙВеёЧтЦзЯдЪОга5жжВЛЭЌРраЭЕФЧтЃЌЧвЗхЕФУцЛ§жЎБШЮЊ2:2:2:l:1ЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНЮЊ
ЁБЃЌЗћКЯЬѕМўЕФЁЊC2H3O2гаЁЊCOOCH3ЁЂЁЊCH2COOHЁЂЁЊCH2OOCHЁЂЁЊOOCCH3ЃЌБНЛЗЩЯЕФЖўИіШЁДњЛљгаСкЁЂМфЁЂЖд3жжЮЛжУЙиЯЕЃЌвђДЫRЕФЭЌЗжвьЙЙЬхга3ЁС4=12жжЃЌЦфжаКЫДХЙВеёЧтЦзЯдЪОга5жжВЛЭЌРраЭЕФЧтЃЌЧвЗхЕФУцЛ§жЎБШЮЊ2:2:2:l:1ЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНЮЊ![]() ЁЂ
ЁЂ![]() ЃЌЙЪД№АИЮЊЃК12ЃЛ
ЃЌЙЪД№АИЮЊЃК12ЃЛ![]() ЁЂ
ЁЂ![]() ЃЛ
ЃЛ
(5)ИљОнЬтИЩСїГЬЭМFЁњGЕФЗДгІЬѕМўПЩжЊЃЌвЊвдСкБНЖўЗг![]() КЭввДМЮЊдСЯжЦБИ
КЭввДМЮЊдСЯжЦБИ![]() ЃЌашвЊЪзЯШКЯГЩ1,2-ЖўТШввЭщЃЌПЩвдгЩввДМЯћШЅєЧЛљКѓгыТШЦјМгГЩМДПЩЃЌвђДЫКЯГЩТЗЯпЮЊ
ЃЌашвЊЪзЯШКЯГЩ1,2-ЖўТШввЭщЃЌПЩвдгЩввДМЯћШЅєЧЛљКѓгыТШЦјМгГЩМДПЩЃЌвђДЫКЯГЩТЗЯпЮЊ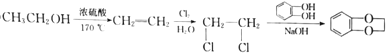 ЃЌЙЪД№АИЮЊЃК
ЃЌЙЪД№АИЮЊЃК ЁЃ
ЁЃ


 ЯАЬтОЋбЁЯЕСаД№АИ
ЯАЬтОЋбЁЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁППЦбЇМвЗЂЯжвЛжжЛЏбЇЪНЮЊH3ЕФЧтЗжзгЃЌдђ1molH3КЭ1molH2ОпгаЯрЭЌЕФЃЈ ЃЉ
A.ЗжзгЪ§B.дзгЪ§C.жЪзгЪ§D.ЕчзгЪ§
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЃЌYОљЕУ1ИіЕчзгДяЕН8eЉЕФЮШЖЈНсЙЙЃЌЧвXЕУЕчзгЗХГіЕФФмСПДѓгкYЕУЕчзгЗХГіЕФФмСПЃЌдђЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
A.XЃЌYЭЌжїзх
B.XдзгЕФАыОЖДѓгкYдзгЕФАыОЖ
C.XЕФЗЧН№ЪєадЧПгкYЕФЗЧН№Ъєад
D.XЉЕФЛЙдадШѕгкYЉЕФЛЙдад
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНќФъРДЃЌЮвЙњЕФЕчзгЙЄвЕбИЫйЗЂеЙЃЌдьГЩСЫДѓСПЕФЕчТЗАхЪДПЬЗЯвКЕФВњЩњКЭХХЗХЁЃЪДПЬвКжївЊгаЫсадЕФ(HCl-H2O2)ЁЂДЋЭГЕФFeCl3аЭ(HCl-FeCl3)ЕШЗНЗЈЃЎЪДПЬЗЯвКжаКЌгаДѓСПЕФCu2+ЃЌЗЯвКЕФЛиЪеРћгУПЩМѕЩйЭзЪдДЕФСїЪЇЃЎМИжжЪДПЬЗЯвКЕФГЃгУДІРэЗНЗЈШчЯТЃК
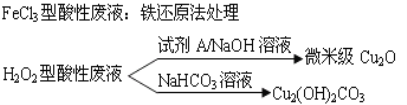
ЃЈ1ЃЉFeCl3аЭЫсадЗЯвКгУЛЙдЗЈДІРэЪЧРћгУFeКЭCl2ЗжБ№зїЮЊЛЙдМСКЭбѕЛЏМСЃЌПЩЛиЪеЭВЂЪЙЪДПЬвКдйЩњЁЃЗЂЩњЕФжївЊЛЏбЇЗДгІгаЃКFe+Cu2+=Fe2++CuЁЂFe+2H+=Fe2++H2ЁќЃЌЛЙга_______________ЁЂ__________________ЃЎ(гУРызгЗНГЬЪНБэЪО)ЁЃ
ЃЈ2ЃЉHCl-H2O2аЭЪДПЬвКЪДПЬЙ§ГЬжаЗЂЩњЕФЛЏбЇЗДгІгУЛЏбЇЗНГЬЪНПЩБэЪОЮЊЃК__________ЁЃ
ЃЈ3ЃЉДІРэH2O2аЭЫсадЗЯвКЛиЪеCu2(OH)2CO3ЕФЙ§ГЬжаашПижЦЗДгІЕФЮТЖШЃЌЕБЮТЖШИпгк80ЁцЪБЃЌВњЦЗбеЩЋЗЂАЕЃЌЦфдвђПЩФмЪЧ____________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏКЯЮяЕФЛЏбЇЪНЮЊ(NH4)2Fe(SO4)2 ЃЌЫќдкЫЎШмвКРяЕчРыЪБЩњГЩСНжжбєРызгКЭвЛжжЫсИљРызг
ЃЈ1ЃЉаДГіСђРызгЕФНсЙЙЪОвтЭМ________________ЃЛ
ЃЈ2ЃЉШєЯђИУЛЏКЯЮяЕФЫЎШмвКжаЭЈШыТШЦјЃЌвЛжжРызгКмШнвзБЛбѕЛЏЃЌИУРызгНЋБфГЩ______ЃЛ(гУРызгЗћКХБэЪО)
ЃЈ3ЃЉШєЯђИУЛЏКЯЮяЕФЫЎШмвКжаМгШыЙ§СПвЛжжМюШмвКЃЌжЛФмЗЂЩњвЛИіРызгЗДгІЃЌдђИУЗДгІЕФРызгЗНГЬЪНЮЊ__________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУЪЕбщЪвГЃгУЕФЮяЦЗ,ИљОнЕчЛЏбЇдРэ,ПЩвдЩшМЦдЕчГиЁЃЧыЬюаДЯТСаПеАз:
(1)ЪЕбщдРэ:Fe+2H+= ЁЃ
(2)ЪЕбщгУЦЗ:ЕчМЋ( ЁЂ )(ЬюЫљгУЕчМЋЕФУћГЦ)ЁЂЯЁСђЫсЁЂЩеБЁЂЕМЯпЁЂЖњЛњ(ЛђЕчСїМЦ)ЁЃ
(3)ЪЕбщзАжУШчЭМЫљЪОЁЃ
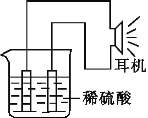
(4)дЕчГиЙЄзїдРэЗжЮі:
ИУдЕчГиЙЄзїЪБ,ИКМЋЮЊ (ЬюЛЏбЇЪН),ЗЂЩњ (ЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБ),ЦфЕчМЋЗДгІЪНЮЊ ,СэвЛЕчМЋЮЊе§МЋ,ЗЂЩњ ЗДгІ,ЦфЕчМЋЗДгІЪНЮЊ ,ЭтЕчТЗжаЕчзгСїЖЏЗНЯђЮЊ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМиЁЂЗњМАаПЕФЯрЙиЛЏКЯЮягУЭОЗЧГЃЙуЗКЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЛљЬЌаПдзгЕФМлЕчзгХХВМЪНЮЊ___________ЃЛKЁЂFЁЂZnЕФЕчИКадДгДѓЕНаЁЕФЫГађЮЊ___________ЁЃ
ЃЈ2ЃЉZnгыCaЮЛгкЭЌвЛжмЦкЧвзюЭтВуЕчзгЪ§ЯрЕШ,ИЦЕФШлЕугыЗаЕуОљБШаПИп,ЦфдвђЪЧ_______________ЁЃ
ЃЈ3ЃЉOF2ЗжзгЕФМИКЮЙЙаЭЮЊ___________ЃЈ1ЗжЃЉ,жааФдзгЕФдгЛЏРраЭЮЊ___________ЁЃ
ЃЈ4ЃЉKOH гыO3ЗДгІПЩЕУЕНKO3(ГєбѕЛЏМи),KO3жаГ§ІвМќЭт,ЛЙДцдк___________ЁЃ
ЃЈ5ЃЉKЁЂFЁЂZnзщГЩЕФвЛжжОЇЬхНсЙЙШчЭМЫљЪО,ЦфОЇАћВЮЪ§ЮЊa=0.4058 nmЁЃ

ЂйОЇАћжаZn2+ЕФХфЮЛЪ§ЮЊ___________ИіЁЃ
ЂкИУОЇЬхЕФУмЖШЮЊ___________(СаГіЫуЪНМДПЩ,гУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕ)gЁЄcm-3ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏбЇЗДгІжаЕФФмСПБфЛЏЪЧШЫРрЛёШЁФмСПЕФживЊЭООЖЁЃ
(1)вКЛЏЦјЪЧвЛжжживЊЕФМвгУШМСЯ,ЯТСаЪОвтЭМгывКЛЏЦјдкШМЩеЙ§ГЬжаЕФФмСПБфЛЏзюЯрЗћЕФЪЧ (ЬюзжФИ)ЁЃ
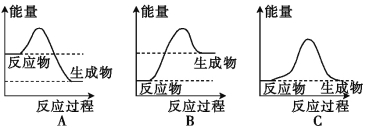
(2)ЁАБљДќЁБПЩгУгкЖЬЪБМфБЃЯЪЪГЮяЁЃНЋвЛЖЈСПЕФЬМЫсФЦОЇЬхгыЯѕЫсяЇОЇЬхУмЗтгквЛЫмСЯДќжа,гУЯпЩўАѓзЁЫмСЯДќжаМфВПЗж,ЪЙСНжжОЇЬхИєПЊ,зіГЩЁАБљДќЁБЁЃЪЙгУЪБНЋЯпЩўНтЯТ,гУЪжНЋДќФкСНжжЙЬЬхЗлФЉГфЗжЛьКЯ,БуСЂМДВњЩњЕЭЮТЁЃгЩДЫХаЖЯ:ЬМЫсФЦОЇЬхгыЯѕЫсяЇОЇЬхЕФзмФмСП (ЬюЁАИпгкЁБЛђЁАЕЭгкЁБ)ЗДгІКѓЩњГЩВњЮяЕФзмФмСПЁЃ
(3)ЛЏбЇЗДгІжаЕФФмСПБфЛЏВЛНіНіБэЯжЮЊШШСПЕФБфЛЏ,гаЪБЛЙПЩвдБэЯжЮЊЦфЫћаЮЪНЕФФмСПБфЛЏЁЃБШШч,РЏжђШМЩеПЩгУРДееУї,етИіЙ§ГЬЪЧНЋЛЏбЇФмзЊЛЏЮЊ КЭ ;ШЫУЧЦеБщЪЙгУЕФИЩЕчГиЙЄзїЪБЪЧНЋЛЏбЇФмзЊЛЏЮЊ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇаЫШЄаЁзщЮЊСЫЬНОПГЃЮТЯТФГЗЧН№ЪєбѕЛЏЮяаЮГЩЕФЮДжЊЦјЬхЕФГЩЗжЁЃИУаЁзщГЩдБНЋЦјЬхЭЈШыГЮЧхЪЏЛвЫЎЃЌЗЂЯжГЮЧхЪЏЛвЫЎБфЛызЧЃЌГжајЭЈШыЗЂЯжЛызЧгжБфГЮЧхЃЌгЩДЫИУаЁзщГЩдБЖдЦјЬхЕФГЩЗжЬсГіВТЯыЁЃ
ЃЈЬсГіВТЯыЃЉ
ВТЯы1ЃК__________________________________ЃЛ
ВТЯы2ЃК__________________________________ЃЛ
ВТЯы3ЃК__________________________________ЁЃ
ЮЊСЫбщжЄВТЯыЃЌИУаЁзщЩшМЦЪЕбщМгвдЬНОПЁЃ
ЃЈЪЕбщЬНОПЃЉ
ИУаЁзщЭЌбЇАДШчЭМЫљЪОзАжУЃЌНЋЦјЬхДгaЖЫЭЈШыЁЃ
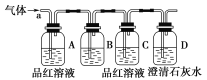
(1)BжагІИУЗХ________ЪдМС(ЬюБрКХ)ЁЃ
aЃЎNaClШмвК BЃЎЫсадKMnO4ШмвК
cЃЎбЮЫс DЃЎГЮЧхЪЏЛвЫЎ
(2)AжаЦЗКьШмвКЕФзїгУЪЧ_________________________________________ЁЃ
(3)DжаГЮЧхЪЏЛвЫЎЕФзїгУЪЧ_______________________________________ЁЃ
ЭЈЙ§ИУЪЕбщЃЌИУаЁзщЭЌбЇЙлВьЕНвдЯТШ§ИіЪЕбщЯжЯѓЃК
ЂйAжаЦЗКьШмвКЭЪЩЋ
ЂкCжаЦЗКьШмвКВЛЭЪЩЋ
ЂлDжаГЮЧхЪЏЛвЫЎБфЛызЧ
ЃЈЕУГіНсТлЃЉ
(4)гЩЩЯЪіЯжЯѓИУаЁзщЭЌбЇШЗШЯИУЦјЬхЮЊ_____________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com