
下列关于原子结构、元素性质的说法正确的是( )
|
| A. | 非金属元素组成的化合物中只含共价键 |
|
| B. | ⅠA族金属元素是同周期中金属性最强的元素 |
|
| C. | 同种元素的原子均有相同的质子数和中子数 |
|
| D. | ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
考点:
原子结构与元素的性质.
专题:
元素周期律与元素周期表专题.
分析:
A、非金属元素组成的化合物可以是离子化合物,如铵盐;
B、同周期自左而右,金属性减弱;
C、同种元素的不同核素质子数相同,中子数不同;
D、阴离子还原性越强,元素的非金属性越弱,最高价氧化物对应水化物的酸性越弱.
解答:
解:A、铵盐是离子化合物,含有离子键,由非金属元素组成,故A错误;
B、同周期自左而右,金属性减弱,故ⅠA族金属元素是同周期中金属性最强的元素,故B正确;
C、同种元素的不同核素质子数相同,中子数不同,故C错误;
D、ⅦA族阴离子还原性越强,元素的非金属性越弱,最高价氧化物对应水化物的酸性越弱,故D错误;
故选B.
点评:
本题考查结构性质位置关系,难度中等,注意对基础知识的理解掌握.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
在2A+B═3C+4D反应中,表示该反应速率最快的是( )
|
| A. | v(A)=0.3mol/(L•s) | B. | v(B)=0.3mol/(L•s) |
|
| C. | v(C)=1.8mol/(L•min) | D. | v(D)=1mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 石油的炼制过程都是化学变化过程
B. 石油分馏目的是将含碳原子数较多的烃先气化经冷凝而分离出来
C. 石油经过常、减压分馏、裂化等工序炼制后即能制得纯净物
D. 石油分馏出来的各馏分仍是多种烃的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 直径介于1~10 nm之间的粒子称为胶体 |
|
| B. | Fe(OH)3胶体是纯净物 |
|
| C. | 利用丁达尔效应可以区别溶液与胶体 |
|
| D. | 胶体粒子不可以透过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于离子键、共价键的各种叙述中,下列说法中正确的是( )
|
| A. | 在离子化合物里,只存在离子键,没有共价键 |
|
| B. | 非极性键只存在于双原子的单质分子(如Cl2)中 |
|
| C. | 原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 |
|
| D. | 由不同元素组成的含多个原子的分子里,一定只存在极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据碳酸钠溶于水呈碱性,碳酸钠既属于盐,又属于碱
② 根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
③ 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和悬浊液
④ 根据反应中是否有离子反应参与,将反应反应分为离子反应和非离子反应
| A.①③ | B.②④ | C.①④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原滴定与酸碱中和滴定一样是化学实验室常用的定量测定方法。某氧化还 原滴定的反应体系中有反应物和生成物共六种, 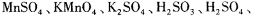
 ,其中H 2 SO 3 的还原性最强,KMnO 4 的氧化性最强。对此反应体系:
,其中H 2 SO 3 的还原性最强,KMnO 4 的氧化性最强。对此反应体系:
(1) 被氧化的元素是_______;发生还原反应的过程是________→______。
(2) 请用这六种物质组织一个合理的化学反应,写出它的离子方程式:_______
(3) 反应中H 2 SO 4 是_______ (填编号)
A,氧化剂 B.氧化产物 C.生成物 D.反应物
(4) 当有20mL 0.1mol/L的氧化剂参加反应时,电子转移数目是_______ 。
(5) 用标准KMnO 4 溶液滴定H 2 SO 3 时,滴定终点时颜色变化是_______。
(6) 滴定过程中.下列图像所表示的关系正确的是_______(填编号)。 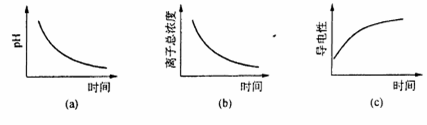
查看答案和解析>>
科目:高中化学 来源: 题型:
H2O2溶液发生分解反应:2H2O2=O2↑+2H2O,在其他条件都相同的情况下,下列反应温度中氧气生成速率最大的是( )
A. 80℃ B. 60℃ C. 40℃ D. 20℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com