
| 编号 | a | b |
| 试剂 | 0.1mol/L Fe(NO3)3 | 0.05mol/L Fe2(SO4)3 |
| 现象 | 银镜消失较快; 溶液黄色略变浅; 产生少许白色沉淀 | 银镜消失较慢; 溶液黄色明显变浅; 产生较多白色沉淀 |
| 实验方案 | 预期现象和结论 |
分析 (1)硝酸银溶液中加氨水,至生成的沉淀恰好溶解可得到银氨溶液;
(2)对照试验中,0.1mol/L Fe(NO3)3和0.05mol/L Fe2(SO4)3中c(Fe3+)是一样的;
(3)Fe3+具有氧化性,金属银具有还原性,Fe3+氧化Ag得到亚铁离子和银离子;
(4)硫酸根离子可以和钡离子之间反应生成白色不溶于硝酸的沉淀硫酸钡,据此检验硫酸根离子;
(5)根据实验信息:a中溶液黄色略变浅,b中溶液黄色明显变浅得到实验结论;
(6)碘化银是一种黄色沉淀,结合亚硝酸盐能与酸化的KI溶液反应来判断沉淀的组成即可.
解答 解:(1)硝酸银溶液中加氨水,至生成的沉淀恰好溶解可得到银氨溶液,所以配制银氨溶液,需要的试剂是AgNO3溶液、稀氨水,故答案为:AgNO3溶液、稀氨水;
(2)分别向两支银镜的试管中加入5mL Fe(NO3)3、Fe2(SO4)3溶液,保证铁离子浓度相等的前提下,来判断银镜溶解的速度,故答案为:c(Fe3+);
(3)Fe3+具有氧化性,金属银具有还原性,Fe3+氧化Ag得到亚铁离子和银离子,即:Fe3++Ag═Fe2++Ag+,故答案为:Fe3++Ag═Fe2++Ag+;
(4)硫酸根离子可以和钡离子之间反应生成白色不溶于硝酸的沉淀硫酸钡,检验硫酸银中硫酸根离子的方法:取少量Ag2SO4固体于试管中,加入适量蒸馏水,振荡、静置,取上层清液,滴加Ba(NO3)2溶液,出现白色沉淀,
故答案为:取少量Ag2SO4固体于试管中,加入适量蒸馏水,振荡、静置,取上层清液,滴加Ba(NO3)2溶液,出现白色沉淀;
(5)根据选择的铁盐溶液铁离子浓度相等,但是盐溶液中的阴离子硝酸根离子和硫酸根离子的不同,单质银镜的溶解情况不同,a中溶液黄色略变浅,b中溶液黄色明显变浅,得到在a中的酸性条件下NO3-氧化了银,0.1mol/L Fe(NO3)3中,硝酸根离子是0.3mol/L,所以配制pH=2,c(NO3-)=0.3mol/L的溶液,结果银镜消失溶液的颜色无变化,说明铁离子没有参加反应,证明a中的酸性条件下NO3-氧化了银,
故答案为:a中溶液黄色略变浅,b中溶液黄色明显变浅;配制pH=2,c(NO3-)=0.3mol/L的溶液;银镜消失,溶液颜色无明显变化;
(6)碘化银是一种黄色沉淀,亚硝酸盐能与酸化的KI溶液反应产生黄色沉淀,亚硝酸具有氧化性,能将碘离子氧化,含有碘单质的溶液中滴加淀粉溶液后变蓝(或CCl4层显紫色),据此确定白色沉淀是否是亚硝酸银,故答案为:
| 实验方案 | 预期现象和结论 | |
| 方案 | 取少量白色沉淀,向其中加入过量酸化的KI溶液,静置,再向上层清液中滴加淀粉溶液(或取上层清液,加入CCl4后振荡、静置) | 加入酸化的KI溶液后产生黄色沉淀,上层清液滴加淀粉溶液后变蓝(或CCl4层显紫色),假设2成立 |
点评 本题考查了物质的组成实验设计和现象分析判断,题干信息的分析理解是解题关键,注意掌握物质性质,题目难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 碳与水反应吸收131.3 KJ的热量 | |
| B. | 1mol固态焦炭与1mol水蒸气反应产生一氧化碳和氢气,吸收131.3 KJ的热量 | |
| C. | 1mol碳和1mol水反应吸收131.3 KJ的热量 | |
| D. | 固态碳和气态水各1mol反应,放出131.3 KJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液中通入Cl2:Fe2++Cl2→Fe3++2Cl- | |
| B. | AlCl3溶液呈酸性:Al3++3H2O→Al(OH)3+3H+ | |
| C. | Al2(SO4)3溶液加入过量的氨水:Al3++3 NH3•H2O→Al(OH)3↓+3NH4+ | |
| D. | NaOH溶液中滴加少量Ca(HCO3)2溶液:Ca2++HCO3-+OH-→CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
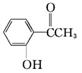 乙:
乙: ,丙:
,丙: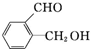
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3的溶解度高于NaCl | |
| B. | KNO3的溶解度低于NaCl | |
| C. | 含有多种杂质时,KNO3比NaCl更适合利用降温结晶(或重结晶)法进行提纯 | |
| D. | 含有多种杂质时,NaCl比KNO3更适合利用降温结晶(或重结晶)法进行提纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C=C | C-C | C≡C | C-H |
| E(kJ/mol) | 436 | 615 | 347.7 | 812 | 413.4 |
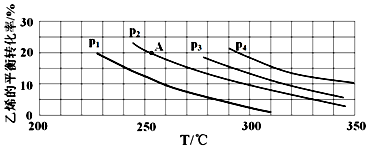
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
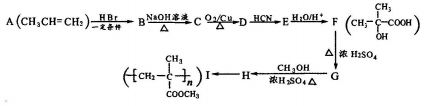
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
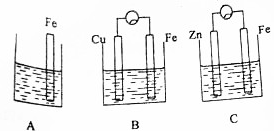 A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com