
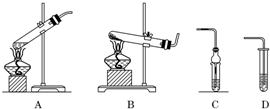
| 实验名称 | 选用的仪器(填字母) | C或D中所盛试剂(填名称) | C或D中的现象 |
| 区别固体Na2CO3和NaHCO3 | BD | 澄清石灰水 | 澄清石灰水变浑浊 |
| 铜和浓硫酸反应 | AC | 品红溶液 | 溶液红色褪去 |
| 制备乙酸乙酯 | AC | 饱和碳酸钠溶液 | 上层有透明油状液体产生并有香味 |
分析 区别固体Na2CO3和NaHCO3,采用加热的方法,分解的气体能使澄清的石灰水变浑浊的为NaHCO3,选用的仪器BD可完成此实验.铜和浓硫酸反应是固液加热的反应,生成的二氧化硫能使品红溶液褪色,选用的仪器AC可完成此实验.制备乙酸乙酯是液液加热的反应,C装置防倒吸,选用的仪器AC可完成此实验.
(1)碳酸氢钠不稳定,加热易分解生成碳酸钠和二氧化碳气体;铜和浓硫酸在加热条件下反应生成具有漂白性的二氧化硫气体;制备乙酸乙酯用乙醇和乙酸在浓硫酸作用下加热制备,用饱和碳酸钠溶液吸收;
(2)A.Cu和浓硫酸反应生成二氧化硫,可与碱反应;
B.根据二氧化硫的漂白性判断;
C.制备乙酸乙酯时,装置C的导管末端在液面以下要防止倒吸现象;
D.实验室可用氯化铵和氢氧化钙制备氨气.
解答 解:(1)碳酸氢钠不稳定,加热易分解生成碳酸钠和二氧化碳气体,可用澄清石灰水检验;
铜和浓硫酸在加热条件下反应生成具有漂白性的二氧化硫气体,可用品红检验;
制备乙酸乙酯用乙醇和乙酸在浓硫酸作用下加热制备,用饱和碳酸钠溶液吸收,
故答案为:
| 澄清石灰水变浑浊 | |||
| 品红溶液 | |||
| AC |
点评 本题综合考查性质实验的方案的设计,题目侧重于物质的制备、检验以及相关物质的性质的考查,题目难度不大,注意相关知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、CO32-、Cl- | B. | K+、H+、Cl-、SO42- | ||
| C. | Na+、Cu2+、SO42-、OH- | D. | H+、K+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
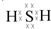 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
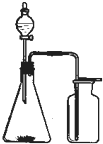 ①浓氨水和固体NaOH制NH3
①浓氨水和固体NaOH制NH3 | A. | ②③ | B. | ①⑥⑦ | C. | ②⑤⑧ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C14H18O4 | B. | C14H16O4 | C. | C14H22O5 | D. | C14H20O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X、Y的简单离子具有相同的电子层结构 | |
| B. | 由Z、W两种元素组成的化合物是离子化合物 | |
| C. | W的简单气态氢化物的热稳定性比X的强 | |
| D. | 离子半径:r(X)<r(Y)<r(Z)<r(W) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com