

| A. | M的化学性质活泼 | B. | L中的化学键是极性键 | ||
| C. | E能使紫色的石蕊试液变蓝 | D. | G是最活泼的非金属单质 |
分析 由反应物和生成物的结构式可知,G、M为单质,E、L为化合物,M为含有3个共用电子对的单质,应为N2,则E为NH3,G可能为F2,也可能为Cl2,二者都能与NH3发生反应,有原子半径的大小可知,G应为F2,则L为HF,以此解答该题.
解答 解:由反应物和生成物的结构式可知,G、M为单质,E、L为化合物,M为含有3个共用电子对的单质,应为N2,则E为NH3,G可能为F2,也可能为Cl2,二者都能与NH3发生反应,有原子半径的大小可知,G应为F2,则L为HF,则
A.M为N2,由于单质的键能较大,性质不活泼,故A错误;
B.L为HF,含有极性共价键,故B正确;
C.E为NH3,溶液呈碱性,能使紫色石蕊试液变蓝色,故C正确;
D.F的非金属性最强,则对应的F2单质是最活泼的非金属单质,故D正确;
故选A.
点评 本题考查无机物的推断,题目难度中等,本题注意根据分子的结构示意图判断物质的种类为解答该题的关键.


科目:高中化学 来源: 题型:选择题
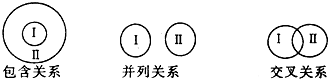
| A. | 电解质与非电解质属于包含关系 | |
| B. | 化合物与碱性氧化物属于包含关系 | |
| C. | 单质与化合物属于交叉关系 | |
| D. | 氧化还原反应与分解反应属于并列关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用碳酸氢钠治疗胃酸过多 | |
| B. | 用双氧水给伤口清洗和消毒 | |
| C. | 用盐酸除去铁锈 | |
| D. | 用溶有碘化钾的淀粉试纸检验某装置是否漏出氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、K+、Cl-、CO32- | B. | Na+、HCO3-、K+、OH- | ||
| C. | K+、Ag+、Cl-、NO3- | D. | Na+、SO42-、K+、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3 | B. | HCO3- | C. | NH4+ | D. | SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制).
用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 对于如图所示的有机化合物的说法,正确的有①②③④⑦.
对于如图所示的有机化合物的说法,正确的有①②③④⑦.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8 g苯含有碳碳双键的数目为0.3NA | |
| B. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA | |
| C. | 273K、101kPa下,28 g乙烯与丙烯混合物中含有C-H键的数目为5NA | |
| D. | 100 mL1mol•L-1的NaF中:N(F-)+N(HF)=0.1 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com