


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
A、1 mol
| ||
| B、3.6 g石墨和C60的混合物中,含有的碳原子数为0.3NA | ||
| C、含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | ||
| D、标准状况下,4.48 L戊烷含有的分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
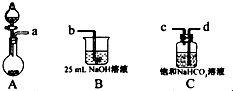 研究碳及其化合物的性质和用途是中学化学的任务之一.
研究碳及其化合物的性质和用途是中学化学的任务之一.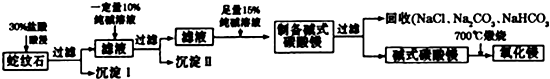
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
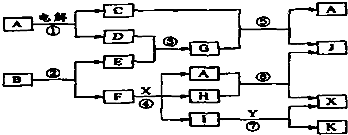
| 元素 | A | B | C | D | E |
| 化合价 | -4 | -3 | -2 | +1 | -1 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A.化学常识 | B.化学与食品 |
| ?空气的主要成分--氮气和氧气 ?硬 水 和 软 水--可用肥皂水来检验 | ?甲 醛--浸泡肉类食品,以防变质 ?工业盐--用来腌制凉果、酸菜等食物 |
| C.化学与生活 | D.化学与能源 |
| ?人体缺铁--会引起贫血症 ?化纤织物、纯毛织物--用灼烧闻气味来鉴别 | ?沼气、酒精--生物能源,可再生能源 ?石 油、煤--化石能源,不可再生能源 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH2=CH-CH=CH2 |
| B、CH2=CH-CH3 |
| C、CH2=CH2 |
| D、以上答案均不合理 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com