
分析 根据n=$\frac{V}{{V}_{m}}$计算标准状况下22.4L氯气的物质的量,
(1)根据方程式定比关系计算参加反应二氧化锰的物质的量,根据m=nM计算二氧化锰的质量;
(2)根据方程式定比关系计算参加反应的HCl的物质的量;
(3)根据c=$\frac{1000ρw}{M}$计算该浓盐酸的物质的量浓度.
解答 解:标准状况下22.4L氯气的物质的量1mol,
(1)令参加反应二氧化锰的物质的量为xmol,则:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O
1mol 1mol
xmol 1mol
故x=1,故参加反应二氧化锰的质量为1mol×87g/mol=87g,
答:参加反应的二氧化锰的质量为87g;
(2)令参加反应的HCl的物质的量为ymol,则:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O
4mol 1mol
ymol 1mol
故y=4mol,被氧化的HCl的物质的量为2mol,
答:被氧化的HCl的物质的量为2mol;
(3)该浓盐酸的物质的量浓度=$\frac{1000×1.19×36.5%}{36.5}$mol/L=11.9mol/L,
答:该浓盐酸的物质的量浓度为11.9mol/L.
点评 本题考查根据方程式的计算、物质的量浓度计算,难度不大,(3)注意掌握物质的量浓度与质量分数的关系.


科目:高中化学 来源: 题型:选择题
| A. | CH3COOH HCl CH3COONa | B. | HCl CH3COOH NaHCO3 | ||
| C. | NH4Cl CH3COOH NaOH | D. | NH4Cl HCl CH3COONa |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠是氧化剂,水是还原剂 | B. | Na2O2是还原剂,水是氧化剂 | ||
| C. | 过氧化钠既是氧化剂又是还原剂 | D. | 水既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 盐酸 | B. | KHS溶液 | C. | NaOH溶液 | D. | Na2S溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
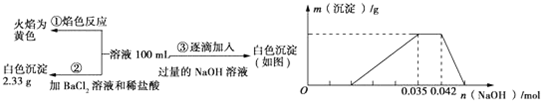
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com