
【题目】密闭容器中有如下反应:mA(g)+nB(g)![]() pC(g)达到平衡后,保持温度不变,将容器体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.8倍。下列说法中正确的是
pC(g)达到平衡后,保持温度不变,将容器体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.8倍。下列说法中正确的是
A.m+n>p B.A的转化率降低
C.平衡向正反应方向移动 D.C的质量分数增加
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图甲是利用一种微生物将废水中的尿素[CO(NH2)2] 的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜。下列说法中正确的是

A. 铜电极应与X相连接
B. H+进过质子交换膜由右向左移动
C. 当N电极消耗0.25mol气体时,则铁电极增重16g
D. M电极反应式:CO(NH2)2+H2O-6e-=CO2↑+N2↑+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
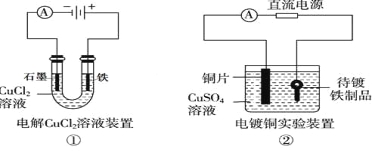
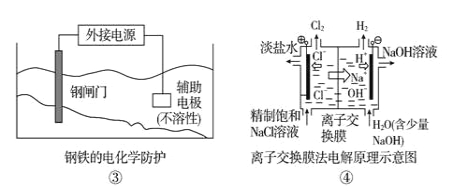
A. ①中阳极处能产生使湿润淀粉KI试纸变蓝的气体
B. ②中待镀铁制品应与电源正极相连
C. ③中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法
D. ④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是元素周期表前四周期中原子序数依次增大的六种常见元素,其相关信息如下表:
元素 | 相 关 信 息 |
A | 原子核外有7种运动状态不同的电子 |
B | 外围电子排布式为nsnnpn+2 |
C | 常见的金属,在周期表中周期序数与族序数相等 |
D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
E | 一种核素的质量数为56,中子数为30 |
F | 单质紫红色,电缆材料,常见氧化物为黑色 |
回答下列问题:
(1)元素E在元素周期表中的位于第四周期第__族,其高价态离子核外有__个未成对电子
(2)B、C、D三种元素的离子半径由小到大的顺序是______(用离子符号表示).
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为_______
(4)常温下AD3是一种淡黄色液体。以下关于AD3的说法中,正确的是__________
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为___________________
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是__________;该过程总的离子反应式为________________向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是________
A.配位键 B.极性共价键 C.非极性共价键 D.离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H10O3并能使新制Cu(OH)2悬浊液溶解,继续加热会出现砖红色沉淀的有机物有(不含立体异构)( )
A.3种
B.4种
C.5种
D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各原子或离子的电子排布式错误的是 ( )
A. Na+: 1s22s22p6 B. F :1s22s22p5
C. O2—: 1s22s22p4 D. Ar: 1s22s22p63s23p6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,1 molL-1的HClO2和1molL-1的HMnO4两种酸溶液,起始时的体积均为V0,分别向两溶液加水稀释至体积V,所得曲线如图所示,下列说法正确的是

A. 酸性:HClO2>HMnO4
B. 稀释前分别用1molL-1的NaOH溶液中和,消耗的NaOH溶液体积: HMnO4 >HClO2
C. 当稀释至pH均为3时,溶液中c(ClO2-)>c(MnO4-)
D. 在0≤pH≤5时,HMnO4溶液满足:pH=lg![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com