
”¾ĢāÄæ”æĖę×ÅČĖĆĒµÄĪļÖŹÉś»īĖ®Ę½µÄ²»¶ĻĢįøßŗĶ¹¤Ņµ»ÆæģĖŁ·¢Õ¹£¬»·¾³ĪŪČ¾Ņ²ČÕŅę¼ÓÖŲ£¬æÕĘųÖŠÓŠ¶¾ĘųĢåÖ÷ŅŖ°üĄØSO2”¢CO”¢NOx”¢ĢžĄąµČµČ”£
£Ø1£©ŌŚø“ŗĻ×é·Ö“߻ƼĮ×÷ÓĆĻĀ£¬CH4æÉŹ¹SO2×Ŗ»ÆĪŖS£¬Ķ¬Ź±Éś³ÉCO2ŗĶĖ®”£ŅŃÖŖCH4ŗĶSµÄČ¼ÉÕČȦ¤H·Ö±šĪŖ-890 kJ/molŗĶ-297kJ/mol£¬ŌņCH4ŗĶSO2·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ_________________________________________”£
£Ø2£©ŌŚ20 LµÄĆܱÕČŻĘ÷ÖŠ°“ĪļÖŹµÄĮæÖ®±Č1”Ć2³äČėCOŗĶH2£¬·¢Éś·“Ó¦£ŗCO(g)£«2H2(g)![]() CH3OH(g) ¦¤H”£²āµĆCOµÄ×Ŗ»ÆĀŹĖęĪĀ¶Č¼°²»Ķ¬Ń¹ĒæµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬P2ŗĶ195 ”ꏱn(H2)Ėꏱ¼äµÄ±ä»Æ½į¹ūČē±ķĖłŹ¾”£
CH3OH(g) ¦¤H”£²āµĆCOµÄ×Ŗ»ÆĀŹĖęĪĀ¶Č¼°²»Ķ¬Ń¹ĒæµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬P2ŗĶ195 ”ꏱn(H2)Ėꏱ¼äµÄ±ä»Æ½į¹ūČē±ķĖłŹ¾”£
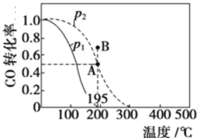
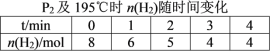
¢ŁP2¼°195”ęĻĀ£¬ŌŚBµćŹ±£¬v(Õż)_____v(Äę)£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©”£
¢ŚøĆ·“Ó¦µÄ¦¤H_________0£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©£¬ŌŅņŹĒ______________________________”£
¢ŪŌŚ0”«2 min£¬Ę½¾ł·“Ó¦ĖŁĀŹv(CH3OH)£½______________________”££ØŹżÖµÓĆŠ”ŹżŠĪŹ½±ķŹ¾£©
¢ÜŌŚP2¼°195 ”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżKp=__________ (ÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č¼ĘĖć£¬·ÖŃ¹=×ÜŃ¹”ĮĪļÖŹµÄĮæ·ÖŹż£¬½į¹ūÓĆŗ¬P2µÄ·ÖŹ½±ķŹ¾)”£
£Ø3£©Ä³ÖÖČŪČŚĢ¼ĖįŃĪČ¼ĮĻµē³ŲŅŌLi2CO3”¢K2CO3ĪŖµē½āÖŹ”¢ŅŌCH4ĪŖČ¼ĮĻŹ±£¬øƵē³Ų¹¤×÷ŌĄķ¼ūĶ¼ĖłŹ¾”£
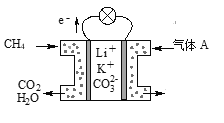
¢ŁĘųĢåAÖŠ³żĮĖO2Ķā£¬Ņ»¶Ø»¹ŗ¬ÓŠµÄĘųĢåŹĒ________”£
¢ŚøƵē³ŲµÄøŗ¼«·“Ó¦Ź½ĪŖ__________________________”£
”¾“š°ø”æCH4 (g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) ”÷H= -296 kJ/mol < < ĘäĖūĢõ¼ž²»±äŹ±£¬ÉżøßĪĀ¶Č£¬Ņ»Ńõ»ÆĢ¼µÄ×Ŗ»ÆĀŹ½µµĶ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖµĆ÷Äę·“Ó¦·½ĻņĪŖĪüČČ£¬Õż·“Ó¦·½Ļņ·ÅČČ 0.0375 mol”¤L£1 min£1 9/P22 CO2»ņ¶žŃõ»ÆĢ¼ CH4-8e-+4CO32-=5CO2+2H2O
”¾½āĪö”æ
£Ø1£©CH4ŗĶSO2·“Ӧɜ³ÉS”¢CO2ŗĶĖ®£¬øł¾ŻCH4ŗĶSµÄČ¼ÉÕČČ»Æѧ·½³ĢŹ½¼ĘĖćĖłĒó·“Ó¦µÄ”÷H £»
£Ø2£©¢ŁAµćŹĒĘ½ŗāדĢ¬£¬Bµć×Ŗ»ÆĀŹ“óÓŚAµć£¬Ó¦øĆĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌBµćv£ØÕż£©£¼v£ØÄę£©£»
¢ŚÉżøßĪĀ¶ČŹ±£¬COµÄ×Ŗ»ÆĀŹ½µµĶ£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬ŌņÄęĻņĪŖĪüČČ·“Ó¦£¬¾Ż“Ė·ÖĪö£»
¢ŪKp=P(CH3OH)/P2(H2)”¤P(CO)£¬ĮŠ³öČż¶ĪŹ½£¬±ķŹ¾³öP(CH3OH)”¢P(H2)”¢P(CO)£¬“śČė±ķ“ļŹ½¼“æÉ£»
£Ø3£©øĆŌµē³ŲĪŖ¼×ĶéČ¼ĮĻµē³Ų£¬ĶØČėČ¼ĮĻµÄµē¼«ĪŖøŗ¼«”¢ĶØČėŃõ»Æ¼ĮµÄµē¼«ĪŖÕż¼«”£·Ö±šŠ“³öÕżøŗ¼«·“Ó¦Ź½£¬½įŗĻĮ½¼«²śĪļ½ųŠŠ·ÖĪö£»
£Ø1£©CH4ŗĶSµÄČ¼ÉÕČȦ¤H·Ö±šĪŖ-890 kJ/molŗĶ-297kJ/mol£¬ŌņCH4(g)+2O2(g)=CO2(g)+ 2H2O(l) ¦¤H= -890 kJ/mol ¢Ł£¬S(s)+ O2(g)=SO2(g) ¦¤H= -297kJ/mol ¢Ś£¬¢Ł-2”Į¢ŚµĆ£¬CH4 (g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) ”÷H= -296 kJ/mol£»
£Ø2£©¢Łøł¾Ż±ķÖŠŹż¾ŻÖŖ£¬Ę½ŗāŹ±ĒāĘų×Ŗ»ÆĀŹĪŖ50%£¬µ±æÉÄę·“Ó¦ÖŠ³õŹ¼·“Ó¦ĪļĪļÖŹµÄĮæÖ®±ČµČÓŚĘä¼ĘĮæŹżÖ®±ČŹ±£¬Ęä·“Ó¦Īļ×Ŗ»ÆĀŹĻąµČ£¬ĖłŅŌøĆĪĀ¶ČŗĶŃ¹ĒæĻĀCOµÄ×Ŗ»ÆĀŹĪŖ50%£¬øł¾ŻĶ¼ÖŖ£¬AµćŹĒĘ½ŗāדĢ¬£¬Bµć×Ŗ»ÆĀŹ“óÓŚAµć£¬øĆ·“Ó¦ŌŚøĆĪĀ¶ČŗĶŃ¹ĒæĻĀ“ļµ½Ę½ŗāדĢ¬£¬Ó¦øĆĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌBµćv£ØÕż£©£¼v£ØÄę£©£»
¢ŚÉżøßĪĀ¶ČŹ±£¬COµÄ×Ŗ»ÆĀŹ½µµĶ£¬Ę½ŗāÄęĻņŅĘ¶Æ£¬ŌņÄęĻņĪŖĪüČČ·“Ó¦£¬¹ŹøĆ·“Ó¦µÄ¦¤H<0£»
¢ŪŌŚ0”«2 min£¬Ę½¾ł·“Ó¦ĖŁĀŹv(H2)£½¦¤n/v/¦¤t=3mol/20L/2min=0.075mol”¤L£1 min£1 £¬v(CH3OH)=1/2 v(H2)=0.0375 mol”¤L£1 min£1£»
¢Ü CO(g)£«2H2(g)![]() CH3OH(g)
CH3OH(g)
n0 4mol 8mol 0mol
¦¤n 2mol 4mol 2mol
nĘ½ 2mol 4mol 2mol
ÓÉČż¶ĪŹ½æÉÖŖ£¬·“Ó¦Ē°ŗóĪļÖŹµÄĮæÖ®±Č=3:2£¬ŌņĘ½ŗāŹ±Ń¹ĒæP=2/3P2£¬¹ŹP(CH3OH)=2/3P2”Į2/8=1/6P2£¬P(H2)=1/3P2£¬P(CO)= 1/6P2£¬Kp=P(CH3OH)/P2(H2)”¤P(CO)= 1/6P2/[(1/3P2)2”¤1/6P2]=9/P22;
£Ø3£©øĆŌµē³ŲĪŖ¼×ĶéČ¼ĮĻµē³Ų£¬øł¾ŻĶ¼ĻóÖŠµē×ÓĮ÷ĻņÖŖ£¬×ó±ßµē¼«ĪŖøŗ¼«”¢ÓŅ±ßµē¼«ĪŖÕż¼«”£øŗ¼«·“Ó¦Ź½ĪŖCH4+4CO32--8e-=5CO2+2H2O£¬Õż¼«·“Ó¦Ź½ĪŖO2+2CO2+4e-ØT2CO32-£¬ĖłŅŌĘųĢåAÖŠ³żĮĖO2Ķā£¬Ņ»¶Ø»¹ŗ¬ÓŠµÄĘųĢåŹĒ¶žŃõ»ÆĢ¼£»


 Źī¼ŁĻĪ½ÓÅąÓŽĢ²ÄÕć½¹¤ÉĢ“óѧ³ö°ęÉēĻµĮŠ“š°ø
Źī¼ŁĻĪ½ÓÅąÓŽĢ²ÄÕć½¹¤ÉĢ“óѧ³ö°ęÉēĻµĮŠ“š°ø ŠĄÓļĪÄ»ÆæģĄÖŹī¼ŁÉņŃō³ö°ęÉēĻµĮŠ“š°ø
ŠĄÓļĪÄ»ÆæģĄÖŹī¼ŁÉņŃō³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖH2(g) + I2(g) ![]() 2HI(g) ”÷H < 0£¬ÓŠĻąĶ¬ČŻ»żµÄĆÜ·āČŻĘ÷¼×ŗĶŅŅ£¬¼×ÖŠ¼ÓČėH2ŗĶI2ø÷0.1mol £¬ŅŅÖŠ¼ÓČė0.1mol H2ŗĶ0.2mol I2£¬ĻąĶ¬ĪĀ¶ČĻĀ·Ö±š“ļµ½Ę½ŗā”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(”” )
2HI(g) ”÷H < 0£¬ÓŠĻąĶ¬ČŻ»żµÄĆÜ·āČŻĘ÷¼×ŗĶŅŅ£¬¼×ÖŠ¼ÓČėH2ŗĶI2ø÷0.1mol £¬ŅŅÖŠ¼ÓČė0.1mol H2ŗĶ0.2mol I2£¬ĻąĶ¬ĪĀ¶ČĻĀ·Ö±š“ļµ½Ę½ŗā”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ(”” )
A. ŅŅÖŠ·“Ó¦ĖŁĀŹ±Č¼×ÖŠ·“Ó¦ĖŁĀŹæģ
B. Ę½ŗāŹ±¼×”¢ŅŅĮ½ČŻĘ÷ÖŠ»ģŗĻĪļµÄ×ÜĪļÖŹµÄĮæÖ®±ČĪŖ2:3
C. ČōĘ½ŗāŹ±¼×ÖŠH2µÄ×Ŗ»ÆĀŹĪŖ40%£¬ŌņŅŅÖŠH2µÄ×Ŗ»ÆĀŹ“óÓŚ40%
D. Ę½ŗāŗó£¬ĻņŅŅÖŠŌŁ¼ÓČė0.1mol H2£¬½ØĮ¢ŠĀµÄĘ½ŗāŹ±£¬¼×ŗĶŅŅÖŠH2µÄ°Ł·Öŗ¬Įæ²»ĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ”×éĪŖŃŠ¾æµē»ÆѧŌĄķ£¬Éč¼ĘČēĶ¼×°ÖĆ”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £©

A.aŗĶb²»Į¬½ÓŹ±£¬ĢśĘ¬ÉĻ»įÓŠ½šŹōĶĪö³ö
B.aŗĶbÓƵ¼ĻßĮ¬½ÓŹ±£¬ĶʬÉĻ·¢ÉśµÄ·“Ó¦ĪŖ£ŗCu2£«+2e-= Cu
C.ĪŽĀŪaŗĶbŹĒ·ńĮ¬½Ó£¬ĢśĘ¬¾ł»įČܽā£¬ČÜŅŗ“ÓĄ¶É«Öš½„±ä³ÉĒ³ĀĢÉ«
D.aŗĶbÓƵ¼ĻßĮ¬½ÓŹ±£¬SO42-ĻņĶµē¼«ŅʶÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢś“„Ć½ŹĒÖŲŅŖµÄ“߻ƼĮ£¬COŅ×ÓėĢś“„Ć½×÷ÓƵ¼ÖĀĘ䏧Ȅ“߻ƻīŠŌ£ŗFe+5CO=Fe(CO)5£»³żČ„COµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©C”¢N”¢OµÄµēøŗŠŌÓɓ󵽊”µÄĖ³ŠņĪŖ_________________£¬»łĢ¬FeŌ×ӵļŪµē×ÓÅŲ¼Ķ¼ĪŖ________________”£
£Ø2£©Fe(CO)5ÓÖĆūōŹ»łĢś£¬³£ĪĀĻĀĪŖ»ĘÉ«ÓĶדŅŗĢ壬ŌņFe(CO)5µÄ¾§ĢåĄąŠĶŹĒ__________£¬ÓėCO»„ĪŖµČµē×ÓĢåµÄ·Ö×ӵĵē×ÓŹ½ĪŖ_________________”£
£Ø3£©ÅäŗĻĪļ[Cu(NH3)2]OOCCH3ÖŠĢ¼Ō×ÓµÄŌÓ»ÆĄąŠĶŹĒ_____________£¬ÅäĢåÖŠĢį¹©¹Ā¶Ōµē×ÓµÄŌ×ÓŹĒ___________________________________”£
£Ø4£©ÓĆ[Cu(NH3)2]OOCCH3³żČ„COµÄ·“Ó¦ÖŠ£¬æĻ¶ØÓŠ_______________ŠĪ³É”£
a£®Ąė×Ó¼ü b£®ÅäĪ»¼ü c£®·Ē¼«ŠŌ¼ü d£®§Ņ¼ü
£Ø5£©NaAlH4¾§ĢåµÄ¾§°ūČēĶ¼ £¬ÓėNa£«½ōĮŚĒŅµČ¾ąµÄAlH4£ÓŠ___________øö£»NaAlH4¾§ĢåµÄĆܶČĪŖ_________g”¤cm£3£ØÓĆŗ¬aµÄ“śŹżŹ½±ķŹ¾£©”£
£¬ÓėNa£«½ōĮŚĒŅµČ¾ąµÄAlH4£ÓŠ___________øö£»NaAlH4¾§ĢåµÄĆܶČĪŖ_________g”¤cm£3£ØÓĆŗ¬aµÄ“śŹżŹ½±ķŹ¾£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ4 LĆܱÕČŻĘ÷ÖŠ³äČė6 mol AĘųĢåŗĶ5 mol BĘųĢ壬ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ3A(g)£«B(g)![]() 2C(g)£«xD(g)£¬5 s“ļµ½Ę½ŗā”£“ļµ½Ę½ŗāŹ±£¬Éś³ÉĮĖ2 mol C£¬¾²ā¶ØDµÄÅضČĪŖ0.5 mol”¤L£1£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ( )
2C(g)£«xD(g)£¬5 s“ļµ½Ę½ŗā”£“ļµ½Ę½ŗāŹ±£¬Éś³ÉĮĖ2 mol C£¬¾²ā¶ØDµÄÅضČĪŖ0.5 mol”¤L£1£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ( )
A. x£½1B. BµÄ×Ŗ»ÆĀŹĪŖ20%
C. Ę½ŗāŹ±AµÄÅضČĪŖ1.50 mol”¤L£1D. BµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.2 mol”¤L£1”¤s£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijæĘŃŠČĖŌ±Ģį³öHCHO(¼×Č©£©ÓėO2ŌŚōĒ»łĮ×»ŅŹÆ£ØHAP)±ķĆę“ß»ÆÉś³ÉH2OµÄĄś³Ģ£¬øĆĄś³ĢŹ¾ŅāĶ¼ČēĻĀ£ØĶ¼ÖŠÖ»»³öĮĖ HAPµÄ²æ·Ö½į¹¹£©£ŗ
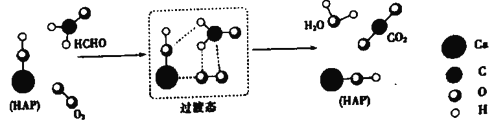
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. HAPÄÜĢįøßHCHOÓėO2µÄ·“Ó¦ĖŁĀŹ
B. HCHOŌŚ·“Ó¦¹ż³ĢÖŠ£¬ÓŠC-H¼ü·¢Éś¶ĻĮŃ
C. øł¾ŻĶ¼Ź¾ŠÅĻ¢£¬CO2·Ö×ÓÖŠµÄŃõŌ×ÓČ«²æĄ“×ŌO2
D. øĆ·“Ó¦æɱķŹ¾ĪŖ£ŗHCHO+O2![]() CO2+H2O
CO2+H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠ²æ·Ö¶ĢÖÜĘŚŌŖĖŲµÄŠŌÖŹ»ņŌ×Ó½į¹¹Čē±ķ£ŗ
ŌŖĖŲ±ąŗÅ | ŌŖĖŲµÄŠŌÖŹ»ņŌ×Ó½į¹¹ |
X | ×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ3±¶ |
Y | ³£ĪĀĻĀµ„ÖŹŹĒĖ«Ō×Ó·Ö×Ó£¬ĘäĒā»ÆĪļµÄĖ®ČÜŅŗĻŌ¼īŠŌ |
Z | µŚČżÖÜĘŚŌŖĖŲµÄ¼ņµ„Ąė×ÓÖŠ°ė¾¶×īŠ” |
(1)ŌŖĖŲXµÄŅ»ÖÖµ„ÖŹŌŚÉś»īÖŠ³£ÓĆ×÷ŅūĖ®»śµÄĻū¶¾¼Į£¬øƵ„ÖŹµÄ»ÆѧŹ½ŹĒ________£¬ŌŖĖŲZµÄĄė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ________”£
(2)ŌŖĖŲYÓėĒāŌŖĖŲŠĪ³ÉŅ»ÖÖĄė×ÓYH![]() £¬ĒėŠ“³öøĆĄė×Óµē×ÓŹ½ __________________”£
£¬ĒėŠ“³öøĆĄė×Óµē×ÓŹ½ __________________”£
(3)Š“³öZŌŖĖŲ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÓėNaOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
___________________________________ӣ
(4)ŌŖĖŲXÓėŌŖĖŲYĻą±Č£¬·Ē½šŹōŠŌ½ĻĒæµÄŹĒ________(ÓĆŌŖĖŲ·ūŗűķŹ¾)£¬ĻĀĮŠ±ķŹöÖŠÄÜÖ¤Ć÷ÕāŅ»ŹĀŹµµÄŹĒ________”£
a£®YµÄĒā»ÆĪļæÉŌŚ“æX2ÖŠČ¼ÉÕÉś³ÉXµÄĒā»ÆĪļŗĶY2
b£®XµÄµ„ÖŹ±ČYµÄµ„ÖŹøüČŻŅ×ÓėH2»ÆŗĻ
c£®XÓėYŠĪ³ÉµÄ»ÆŗĻĪļÖŠYŌŖĖŲ³ŹÕż¼ŪĢ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÕĘųÖŠĘūÓĶŗ¬ĮæµÄ²āĮæŅĒ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾(ÓĆĒæĖįŠŌČÜŅŗ×÷µē½āÖŹČÜŅŗ)”£ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ
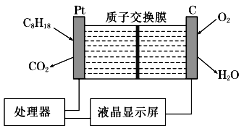
A. ŹÆÄ«µē¼«×÷Õż¼«£¬·¢Éś»¹Ō·“Ó¦
B. ²¬µē¼«µÄµē¼«·“Ó¦Ź½ĪŖC8H18£«16H2O£50e£=8CO2”ü£«50 H£«
C. H£«ÓÉÖŹ×Ó½»»»Ä¤×ó²ąĻņÓŅ²ąĒØŅĘ
D. ĆæĻūŗÄ5.6 L O2£¬µēĀ·ÖŠĶعż1 molµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·“Ó¦N2(g)+O2(g)=2NO(g)µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾”£ŅŃÖŖ£ŗ¶ĻæŖ1mol N2(g)ÖŠ»Æѧ¼üŠčĪüŹÕ946kJÄÜĮ棬¶ĻæŖ1mol O2(g)ÖŠ»Æѧ¼üŠčĪüŹÕ498kJÄÜĮ攣

ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. N2(g)+O2(g)=2NO(g) ”÷H£½-180![]()
B. NO(g)=1/2N2(g)+1/2O2(g) ”÷H£½+90![]()
C. ¶ĻæŖ1mol NO(g)ÖŠ»Æѧ¼üŠčŅŖĪüŹÕ632kJÄÜĮæ
D. ŠĪ³É1 mol NO(g)ÖŠ»Æѧ¼üæÉŹĶ·Å90kJÄÜĮæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com