
【题目】锆(Zr)是40号元素,位于第五周期ⅣB族,锆可溶于氢氟酸和王水,锆及其化合物在陶瓷、耐火材料等多个领域有着重要用途。请回答下列相关问题。
(1)基态锆原子的价电子排布图(轨道表示式)是___。
(2)ZrSiO4和ZrSiO3是锆的两种硅酸盐,二者含有的阳离子Zr4+和Zr2+中比较稳定的是____,原因是___。SiO32-的空间构型是____,SiO42-中的Si原子的杂化类型是____。
(3)[Zr(C2H5O)2]2+是Zr4+形成的一种配离子,其中的配位原子是___(填元素符号),该离子中含有的化学键种类不包括___(填选项序号)。
A.极性键 B.非极性键 C.σ键 D.π键
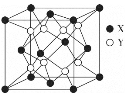
(4)立方氧化锆是一种人工合成的氧化物,由于硬度极高且外观接近钻石常被用作钻石的替代品,其晶胞结构如图所示,立方氧化锆的化学式是___,锆原子的配位数是____。若晶胞中距离最近的两个氧原子间的距离为anm,则立方氧化锆的密度为__g/cm3。
【答案】![]() Zr4+ Zr4+的4d和5s能级均为全空,结构比较稳定 平面三角形 sp3 O D ZrO2 8
Zr4+ Zr4+的4d和5s能级均为全空,结构比较稳定 平面三角形 sp3 O D ZrO2 8 ![]()
【解析】
(1)基态锆原子的价电子排布图(轨道表示式)是![]() ;
;
答案为:![]() ;
;
(2)Zr4+的4d和5s能级均为全空,结构比较稳定,因此Zr4+比Zr2+稳定;根据价层电子理论,SiO32-中心原子价电子对数=![]() ,为sp2杂化,共有4个原子构成,空间构型为平面三角形;SiO42-中的Si原子为中心原子,价电子对数=4,为sp3杂化。
,为sp2杂化,共有4个原子构成,空间构型为平面三角形;SiO42-中的Si原子为中心原子,价电子对数=4,为sp3杂化。
答案为:Zr4+;Zr4+的4d和5s能级均为全空,结构比较稳定;平面三角形;sp3;
(3)配体C2H5O-中只有氧原子含有孤对电子,因此配位原子是O,该离子的结构是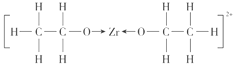 ,其中不含有π键。
,其中不含有π键。
答案为:O;D
(4)根据均摊法可算出晶胞中X原子数目为4,Y原子数目为8,结合锆和氧的常见价态可知其化学式为ZrO2,X为锆原子,其配位数为8。晶胞中距离最近的两个氧原子间的距离为anm,则晶胞棱长为2anm,立方氧化锆的密度![]() 。
。
答案为:ZrO2;8;![]() ;
;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件略,有些反应的产物和反应的条件没有全部标出)。已知A、B、E是单质,其中A着火只能用干燥的沙土灭火,B在常温下为气体,C俗名称为烧碱,D为无色无味液体。

(1)写出A、B、F的化学式 A______ B ______ F ______。
(2)写出A和D反应生成B和C的化学方程式_____________。若生成3mol的B,则转移的电子数目为_______________ 。
(3)写出E与C、D反应生成的B和F离子方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的有效利用可以缓解温室效应和能源短缺问题。
(1)CO2的分子结构决定了其性质和用途。
①CO2的电子式是_____________。
②在温度高于31.26 ℃、压强高于7.29×106Pa时,CO2处于超临界状态,称为超临界CO2流体,它可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,用超临界CO2萃取的优点有:___________(答出一点即可)。
(2)中科院大连化学物理研究所的科研人员在新型纳米催化剂Na-Fe3O4和HMCM-22 的表面将CO2转化为烷烃,其过程如下图。

上图中CO2转化为CO的反应为:CO2(g)+H2(g) = CO(g)+H2O(g) △H= +41kJ/mol
已知:2CO2(g)+6H2(g) = C2H4(g)+4H2O(g) △H= -128kJ/mol
①则图中CO转化为C2H4的热化学方程式是____________________。
②关于X与Y的说法正确的是________(填序号〕。
a.实验式相同 b.都有4种一氯代物
c.都易使酸性KMnO4溶液褪色 d.互为同系物
③催化剂中Fe3O4的制备方法如下:将一定比例的FeCl2和FeCl3溶于盐酸,然后在 60 ℃下逐滴加入NaOH溶液至pH≈10,继续搅拌,得Fe3O4。该反应的离子方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(MnS)=2.5×10-13,常温下三种物质在水中的沉淀溶解平衡线如图所示(X表示Fe、Cu、Mn)。下列说法正确的是

A. 曲线Ⅰ表示CuS的溶解平衡曲线
B. MnS在a点溶液中的溶度积等于在b点溶液中的溶度积
C. c点与d点溶液中S2-的物质的量浓度相等
D. 向含有XS固体的d点溶液中滴加稀硫酸至过量可使固体逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯(结构如图1所示)是食品行业中常用的一种香精,柠檬烯熔点为-74.3℃,沸点为177℃,难溶于水,在接近100℃时有一定的挥发性。柠檬、橙子和柚子等水果果皮中存在较多的柠檬烯,实验室通常用水蒸气蒸馏(装置如图2所示)的方法将柠檬烯从果皮中提取出来并进行后续的分离提纯。
水蒸气蒸馏:将60g橙子皮剪成碎片投入仪器B中,加入30mL蒸馏水,打开T形管活塞,点燃酒精灯加热水蒸气发生装置,待T形管支管口有大量水蒸气冒出时关闭活塞并开始通入冷凝水,当D中收集到约60~70mL馏出液时停止蒸馏。
分离提纯:将馏出液倒入分液漏斗,每次用10mL二氯甲烷(沸点39.95℃)萃取三次,萃取液合并后置于锥形瓶中,加入适量无水硫酸镁,半小时后过滤,将滤液进行蒸馏除去二氯甲烷,蒸馏烧瓶中得到主要成分是柠檬烯的橙油。
请回答相关问题。

(1)仪器A的名称是____。安全管下端不能抵住仪器A的底部,原因是__。仪器B中水蒸气导入管管口接近瓶底,目的是___。
(2)直形冷凝管填能否更换为球形冷凝管___(“能”或“否”),原因是___。
(3)分离提纯过程中加入无水硫酸镁的作用是____。对滤液进行蒸馏时合适的加热方法是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出实验过程中总的化学方程式______________;在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是_______反应。(填“吸热”或“放热”).
(2)甲是热水浴,乙是冷水浴,但两个水浴作用不相同,①甲的作用是___________;②乙的作用是____________________________________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还有___________ 。要除去该物质,可先在混合液中加入__________(填写字母),然后再通过蒸馏即可除去。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某磁黄铁矿的主要成分是FexS(S为-2价),既含有Fe2+又含有Fe3+。将一定量的该磁黄铁矿与100 mL的盐酸恰好完全反应(注:矿石中其他成分不与盐酸反应),生成2.4 g硫单质、0.425 mol FeCl2和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是 ( )
A. 100 mL的盐酸中HCl的物质的量浓度为7.5 mol·L-1
B. 生成的H2S气体在标准状况下的体积为2.24 L
C. 该磁黄铁矿FexS中,x=0.85
D. 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】看下列仪器装置图,回答下列问题:
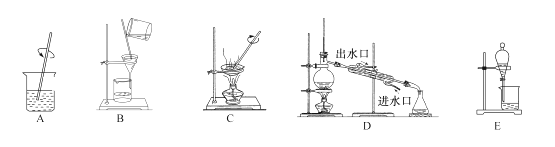
(1)粗盐的提纯需要上面的哪些装置?___________(填字母符号)
(2)分离以下混合物应该选择使用什么装置?(填字母符号)
①酒精和水:___________,
②食盐和水:___________,
③二氧化锰和KCl:___________,
④花生油和水:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组,将一包白色粉末(NaHCO3和Na2CO3的混合物)进行定量分析。现称取一份质量为27.4 g的样品,将此样品加热灼烧至质量不再变化,取出剩余物质,冷却后称重,质量为21.2g。
(1)写出加热时发生反应的化学方程式:___。
(2)分别求出该样品中NaHCO3和Na2CO3的物质的量。____、____(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com