
下列离子方程式书写正确的是
A.碳酸钙跟稀盐酸反应 CO32-+2H+=CO2↑+H2O
B.向碳酸钠溶液中加入过量醋酸溶液 CO32-+2H+=CO2↑+H2O
C.氯气与水反应 Cl2+H2O=2H++Cl-+ClO-
D.三氯化铝溶液与氨水 Al3++3NH3 ·H2O=Al(OH)3↓+3 NH4 +
科目:高中化学 来源: 题型:
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中c(H+)值增大,可以采取的措施是
CH3COO-+H+,要使溶液中c(H+)值增大,可以采取的措施是
A.加少量烧碱溶液 B.加蒸馏水
C.加少量醋酸钠固体 D.升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式2C2H2 (g) + 5O2 (g)= 4CO2 (g) +2H2O (g) ΔH= -1256 kJ/mol,下列说法正确的是
A.乙炔的燃烧热为1256 kJ /mol
B.若转移10 mol电子,则消耗2.5 mol O2
C.若生成2 mol 液态水,则ΔH = -1256 kJ/mol
D.若形成4 mol碳氧共用电子对,则放出的热量为1256 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2 (g) + 3 H2(g)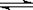 2NH3(g)
2NH3(g)
(1)若反应达平衡时某时刻t时,nt (N2) = 13mol,nt (NH3) = 6mol,计算a的值
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)
为25%。计算平衡时NH3的物质的量。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
n(始)∶n(平) = 。
(4)原混合气体中,a∶b = 。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α (H2)= 。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3) = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C都是金属,把A浸入C的硫酸盐溶液中,A的表面有C析出,A与B和稀硫酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为( )
A.A>B>C B.A>C>B C.B>A>C D.B>C>A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com