
XeF4在水中的反应为:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。下列说法中正确的是
A.XeF4分子中各原子均达到8电子稳定结构
B.XeF4分子中Xe的化合价为0价
C.上述反应中氧化剂和还原剂的物质的量之比为2∶3
D.XeF4按上述方式水解,每生成4 mol Xe,转移16 mol电子
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
已知原子序数,可推断原子的( )
①质子数 ②中子数 ③质量数 ④核电荷数 ⑤核外电子数 ⑥原子结构示意图 ⑦元素在周期表中的位置
A.①②③④⑥ B.①④⑤⑥⑦ C.②③④⑤⑦ D.③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )。
元素代号 | 原子半径/nm | 主要化合价 |
X | 0.160 | +2 |
Y | 0.143 | +3 |
Z | 0.102 | +6、-2 |
L | 0.099 | +7、-1 |
M | 0.077 | +4、-4 |
Q | 0.074 | -2 |
A.等物质的量的X、Y的单质与足量的盐酸反应,生成的H2一样多
B.Y与Q形成的化合物不能跟氢氧化钠溶液反应
C.Z的氢化物的稳定性强于L的氢化物的稳定性
D.在化学反应中,M原子与其他原子易形成共价键而不易形成离子键
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三终极预测理综化学试卷(解析版) 题型:选择题
下列解释实验事实的方程式正确的是
A.Al2(SO4)3溶液滴加氨水产生白色胶状沉淀: Al3++3OH- = Al(OH)3↓
B.90 ℃时,测得纯水中c(H+)·c(OH-) =3.8×10—13: H2O(l)  H+(aq)+OH-(aq) ?H<0
H+(aq)+OH-(aq) ?H<0
C.FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2 +2H2O = 2Fe2++SO42 -+ 4H+
D.碳酸钠溶液滴入酚酞变红:CO32 -+ 2H2O  H2CO3+2OH-
H2CO3+2OH-
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)镍是一种十分重要的有色金属,但粗镍中一般含有Fe、Cu及难与酸、碱溶液反应的不溶性杂质而影响使用。现对粗镍进行提纯,具体的反应流程如下:
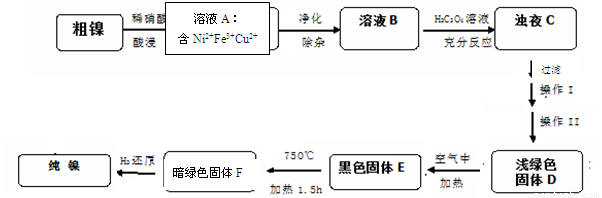
已知:
①2Ni2O3 (黑色)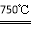 4NiO(暗绿色) + O2↑
4NiO(暗绿色) + O2↑
②
物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
Ksp | 8.8×10-36 | 2.2×10-20 | 5.48×10-16 | 3.2×10-19 |
根据信息回答:
(1)28Ni在周期表中的第 周期;镍与稀硝酸反应的离子方程式为 。实验表明镍的浸出率与温度有关,随着温度升高镍的浸出率增大,但当温度高于70℃ 时,镍的浸出率又降低,浸出渣中Ni(OH)2含量增大,其原因为 ;
(2)在溶液A的净化除杂中,首先将溶液A煮沸,调节PH=5.5,加热煮沸5min,静置一段时间后,过滤出Fe(OH)3。为了得到纯净的溶液B还需要加入以下物质 进行除杂(填正确答案标号)。
A、NaOH B、Na2S C、H2S D、NH3﹒H2O
(3)已知以下三种物质的溶解度关系:NiC2O4>NiC2O4·H2O> NiC2O4·2H2O。则操作I、II名称是 、 ; D生成E的化学方程式为 。
(4)1molE经上述流程得到纯镍,理论上参加反应的氢气为 mol。
(5)测定样品中的镍含量的基本思路是将Ni2+转化为沉淀,通过测量沉淀的质量进一步推算Ni含量。已知Ni2+能与CO32-,C2O42-、S2-等离子形成沉淀,但测定时常选用丁二酮肟(C4H8N2O2)作沉淀剂,生成分子式为C8H14N4O4Ni的鲜红色沉淀。从实验误差角度分析主要原因为: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:简答题
[有机化学基础](15分)
可用来制备抗凝血药,通过下列路线合成: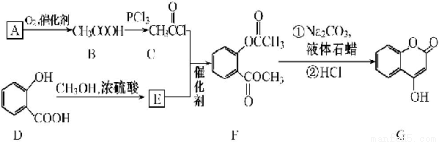
请回答:
(1)B→C的反应类型是____________________。
(2)下列关于化合物G的说法不正确的是_____。
A 分子式是C9H6O3 B 能与金属钠反应
C分子中含有4种官能团 D能与液溴反应
E. 1 mol G最多能和4mol氢气反应 F. 1 mol G最多能和3 molNaOH反应
(3)写出A与银氨溶液反应的化学方程式 。
(4)写出D→E的化学方程式___________________________________________。
(5)写出F和过量NaOH溶液共热时反应的化学方程式_______________________。
(6)化合物E的同分异构体很多,除E外符合下列条件的共 种。
①含苯环且能与氯化铁溶液显色;②苯环上有两个取代基;③含酯基。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
①如果某化合物只含共价键,则其一定是共价化合物
②有阴离子存在的物质中一定存在阳离子
③碳、氮形成的氢化物常温下都是气态
④非金属单质在反应中都只能作氧化剂,具有强氧化性
⑤金属氧化物不一定是碱性氧化物
⑥稀有气体不活泼是因为它们原子最外层都达到8e-稳定结构
A.①②⑤ B.②③④ C.①②⑥ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列物质在一定条件下,可与苯发生化学反应的是
①氯气 ②溴水 ③氧气 ④酸性KMnO4溶液 ⑤KOH溶液
A.①③ B.②③ C.②④ D.①⑤
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列说法中正确的是 ( )
A.一定条件下向1 L容器内通入46 g NO2,则NO2的物质的量浓度一定为1 mol/L
B.标准状况下,22.4L的己烷中有20×6.02 × 1023个原子
C.1 mol氯气溶于水转移6.02× 1023个e—
D.0.1 mol CH5+含6.02 × lO23个e一
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com