
| A. | ${\;}_{1}^{1}$He | B. | ${\;}_{2}^{3}$He | C. | ${\;}_{2}^{5}$He | D. | ${\;}_{2}^{1}$He |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CH(CH3)CH(CH3)2的系统名称是2,3一二甲基丁烷 | |
| B. | 石油化工中裂化是为了提高轻质油的产量和质量 | |
| C. | 维勒在制备氰酸铰时得到了尿素,打破了“生命力论”的统治地位 | |
| D. | 乙醇和浓硫酸加热到170°时发生脱水生成乙醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应Na+2H2O=Na++2OH-+H2↑ | |
| B. | 金属铝溶于氢氧化钠溶液Al+2OH-=AlO2-+H2↑ | |
| C. | 金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ | |
| D. | 铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 热稳定性:PH3>H2S>HCl>H2O | D. | 非金属性:F>O>Cl>Br>I>S |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
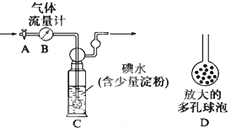 硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com