
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)称取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L,反应的离子方程式为 。
(2)称取同样的a g样品,在高温下恰好完全反应。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比,c:b为_______________。
根据上述实验可确定该铝热剂中含Al的质量分数为 。
 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源:2015-2016学年陕西省高二下期末化学试卷(解析版) 题型:选择题
浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随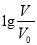 的变化如图所示,下列叙述正确的是( )
的变化如图所示,下列叙述正确的是( )
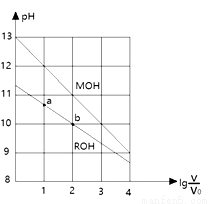
A.MOH的碱性弱于ROH的碱性
B.ROH的电离程度:b点小于a点
C.当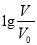 =2时,若两溶液同时降低温度,则c(M+)/c(R+)增大
=2时,若两溶液同时降低温度,则c(M+)/c(R+)增大
D.两溶液无限稀释,它们的c(OH-)永远是MOH>ROH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二6月月考化学试卷(解析版) 题型:填空题
本题为《化学反应原理(选修4)》选做题。
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
(1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈_____性,原因是___________;(用离子方程式表示)
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于___________;
(3)已知在H2S溶液中存在下列平衡:H2S HS-+H+
HS-+H+
①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向______移动,(填“左”或“右”)c(H+)_________。(填“增大”、“减小”或“不变”)
②向H2S溶液中加入NaHS固体时,电离平衡向______移动,(填“左”或“右”)c(S2-)_________。(填“增大”、“减小”或“不变”)
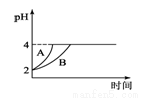
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图1所示.则图中表示醋酸溶液中pH变化曲线的是________(填“A”或“B”);
(5)难溶电解质在水溶液中存在溶解平衡。某MgSO4溶液里c(Mg2+)=0.002mol•L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于________;(该温度下Mg(OH)2的Ksp=2×10-11)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二6月月考化学试卷(解析版) 题型:选择题
CH4与Cl2在光照条件下反应生成多种产物,其中物质的量最大的是
A.HCl B.CCl4 C.CH3Cl D.H2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期末化学试卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源等。下列有关说法正确的是

A.以NaCl为工业原料可以生产烧碱、纯碱以及漂白粉等含氯产品
B.工业上通过电解饱和MgCl2溶液制取金属镁
C.第③④⑤步的目的是浓缩、富集溴单质,这三步中溴元素均被氧化
D.过程①除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期末化学试卷(解析版) 题型:选择题
Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg===Mg2++2Ag+2Cl-。有关该电池的说法正确的是
A.Mg为电池的正极
B.负极反应为AgCl+e-=Ag+Cl-
C.不能被KCl溶液激活
D.可用于海上应急照明供电
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高二上学期期中化学试卷(解析版) 题型:填空题
选择以下物质填写下列空白
A、干冰 B、铜 C、二氧化硅 D、氢氧化钠
(1)晶体中存在分子的是 (填写序号,下同);
(2)晶体中既有离子键又有共价键的是 ;
(3)熔化时需要破坏共价键的是 ;
(4)具有导电、导热、延展性的是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:推断题
钢铁等铁制品是应用最广泛的金属材料,铁元素的单质及其化合物在元素化合物世界始终扮演着重要角色。
I、打磨过的细铁丝可在纯氧中剧烈燃烧,最终生成黑色固体;铁粉与水蒸气在高温下也可生成该黑色固体,
(1)反应的化学方程式为 。
(2)将该黑色固体溶于盐酸中,反应的离子反应方程式 。
II、某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下:
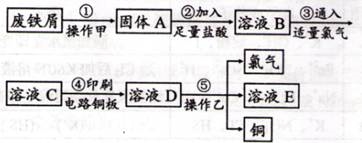
请回答下列问题:
(1)步骤②中,除发生反应Fe +2HCl=FeCl 2 +H 2 ↑外,其他可能反应的离子方程式为 。
(2)若将③该加H2O2 书写离子反应方程式 。
(3)若溶液B中只含有Fe 2+ 而不含Fe 3+ ,可证明该事实的实验方法是( )
①先加氯水,后加KSCN溶液后显红色;
②先加KSCN溶液,不显红色,再加氯水后显红色;
③滴加NaOH溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色;
④只滴加KSCN溶液不显红色。
A.①② B、②③ C、③④ D、①④
(4)步骤④化学方程式为 。
(5)若除去氯化铜中氯化铁可以加入剂 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com