
氧化还原反应中实际上包含氧 化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+2H2O,已知KMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+2H2O,已知KMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式: 。
(2)反应中硝酸体现了 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年黑龙江省高一12月月考化学试卷(解析版) 题型:实验题
某校化学小组学生利用下图所列装置进行“铁与水反应”的实验并进行产物的检验。(图中夹持及尾气处理装置均已略去)
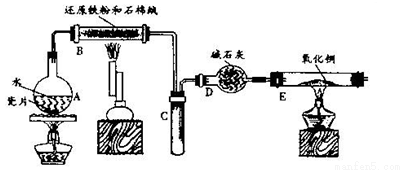
(1)烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 。装置B中发生反应的化学方程式是 。
(2)如果要在C处玻璃管处点燃该气体,则必须对该气体进行 , 装置E中的现象是 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法____________________。
(4)若(3)实验中未检验到Fe3+的存在, 则可能的原因是______________(用离子方程式表示)。继续向溶液中滴加NaOH溶液,观察到的实验现象是 ,写出该过程中涉及到的化学方程式 、 。
则可能的原因是______________(用离子方程式表示)。继续向溶液中滴加NaOH溶液,观察到的实验现象是 ,写出该过程中涉及到的化学方程式 、 。
(5)若(3)实验中检验到Fe3+的存在,向溶液中通入一定量的SO2,观察到溶液由黄色变为浅绿色,写出反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考四化学卷(解析版) 题型:选择题
若以NA代表阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol Na 跟足量H2O反应得到电子的数目为NA
B.常温常压下,16 g甲烷(CH4)所含电子数为NA
C.标准状况下,22.4 L 酒精所含的分子数目为NA
D.常温常压下,6 g O2和26 g O3混合气体中的原子总数为2NA
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三12月月考化学试卷(解析版) 题型:选择题
X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具有相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍。下列说法正确的是
A. X与Y形成的化合物只有一种 B. 原子半径:r(Z)<r(R)
C. R的氢化物的热稳定性比W的强 D. R的氧化物对应水化物的酸性比W的强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:计算题
取1.43gNa2CO3•XH2O晶体溶于水,配成10.0mL溶液。然后逐滴滴入稀盐酸直至没有气体放出为止,共用去盐酸20.0mL,并收集到112mLCO2(标况)。
计算:(1)稀盐酸的物质的量浓度;
(2)Na2CO3•XH2O的摩尔质量;(3)X的值。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
实验室要用98%(ρ=1.84g·cm-3)的硫酸配制3.68mol·L-1的硫酸溶液500mL,若其他操作均正确,但出现下列错误操作,所配制的硫酸溶液浓度偏高的是
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
等体积硫酸铝、硫酸锌、硫酸钠溶液分别与足量的氯化钡溶液反应。若生成的硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐溶液的物质的量浓度比为
A.1:2:3 B.1:6:9 C.1:3:3 D.1:3:6
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上月考二化学卷(解析版) 题型:填空题
向浓度相等、体积均为50 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的CO2后,再稀释到100 mL。
(1)在 NaOH 溶液中通入一定量的 CO2 后,溶液中溶质的可能组成是
①_________, ②________, ③________, ④________。
(2)在稀释后的溶液中逐滴加入0.2 mol/L 的盐酸,产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
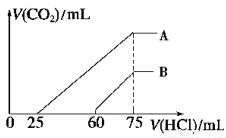
①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生 CO2 的最大体积是_________mL(标准状况)。
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________。
③原 NaOH 溶液的物质的量浓度为________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二12月检测化学试卷(解析版) 题型:填空题
现有常温条件下甲、乙、丙三种溶液,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的盐酸,丙为未知浓度的FeCl2溶液,试回答下列问题:
(1) 甲溶液的pH= 。
(2) 丙溶液中存在的化学平衡有 (用离子方程式表示)。
(3) 甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com