
 W��Q��R��X��Y��Z����ԭ���������ε���������Ԫ�أ���֪W��Y�ĵ����ڳ����������壻QW4������һ����������Y�ĵ���������Ӧ�����������ֲ��R��Y��Z��Y�����γ����Ӹ�����Ϊ1��1�ľ��壬�������־����У�ÿ��Y����������R������Z���ӵĸ�����Ϊ3��4��X�ĵ���һ������������Q������������о���ȼ�գ���ش��������⣺
W��Q��R��X��Y��Z����ԭ���������ε���������Ԫ�أ���֪W��Y�ĵ����ڳ����������壻QW4������һ����������Y�ĵ���������Ӧ�����������ֲ��R��Y��Z��Y�����γ����Ӹ�����Ϊ1��1�ľ��壬�������־����У�ÿ��Y����������R������Z���ӵĸ�����Ϊ3��4��X�ĵ���һ������������Q������������о���ȼ�գ���ش��������⣺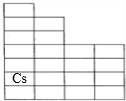 ��
�� ��
��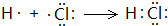 ����H��C����Ԫ����ɵ�16���ӷ���ΪC2H4����ṹʽΪ
����H��C����Ԫ����ɵ�16���ӷ���ΪC2H4����ṹʽΪ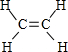 ��
��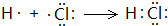 ��
��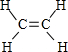 ��
��| 1mol��40g/mol |
| 20g |
| 1 |
| 2 |
| 1 |
| 2 |


 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe3+��Ba2+��OH-��NO3- |
| B��Ba2+��Na+��SO42-��0H- |
| C��K+��Al3+��NO3-��Cl- |
| D��H+��K+��CO32-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��Na+����c��HSO3-����c��H2SO3����c��SO32-�� |
| B��c��Na+����c��HSO3-��+c��SO32-�� |
| C��c��Na+��+c��H+��=2c��SO32-�� |
| D��c��Na+��+c��H+��=c��HSO3-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��22.4L O2�����ķ�����ĿΪNA |
| B��36.5g HCl���е�ԭ����ĿΪ2NA |
| C��1mol CO2���еķ�����ĿΪNA |
| D��500mL 1mol?L-1���Ȼ�����Һ�к�����������ĿΪ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��22.4L��CO�����1mol N2�����ĵ�������� |
| B��1L�ܶ�Ϊ1.84g?cm-3��������Ϊ98%��������Һ�У�������ԭ����Ϊ36.8NA |
| C���ڱ�״���£�32g�����ͳ����Ļ�������к���ԭ����Ϊ2NA |
| D��1mol/L FeCl3 ��Һ�У�����Cl-����ĿΪ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����1mol/L�� AlCl3��Һ�У�A13+�ĸ���С��NA | ||
| B��1mol̼ϩ����CH2���к��е�����Ϊ8NA | ||
C����״���£�1L����ķ�����Ϊ
| ||
| D��1mol C4H10�����к��еĹ��ۼ�����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Ƶ�ˮ�ⷴӦ��S2-+2H2O?H2S+2OH- |
| B����Ƭ������������Һ��Ӧ��Al+2OH-�TAlO2-+H2 |
| C��������������Һ��ͨ��������4Fe2++O2+4H+�T4Fe3++2OH- |
| D�������������Һ��ͨ������SO2���壺ClO-+SO2+H2O�THClO+HSO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������NaOH��Һ��Al+2OH-�TAlO2-+H2�� |
| B��ͭ����ϡ���3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O |
| C��̼��þ�еμ�ϡ���CO32-+2H+�TCO2��+H2O |
| D��ϡ�����еμ�����������Һ��H++OH-�TH2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com