
|
如图所示,不同温度和压强下,在固定容积的密闭容器中对可逆反应: 4L(g) 平衡状态的影响(p1>p2),图中Y轴可以表示的涵义是:
| |
| [ ] | |
A. |
体系中物质L的百分含量 |
B. |
体系中总的气体分子数目 |
C. |
气体混合物的平均相对分子质量 |
D. |
气体混合物的密度 |
科目:高中化学 来源: 题型:阅读理解
 合成氨工业对国民经济和社会发展具有重要的意义.其原理为:
合成氨工业对国民经济和社会发展具有重要的意义.其原理为:| c(H2)?c(CO) |
| c(H2O) |
| c(H2)?c(CO) |
| c(H2O) |
| 实验组别 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 2 | 900 | 0.5 | 1 | 0.2 | 0.8 | 3 |
| 3 | T | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
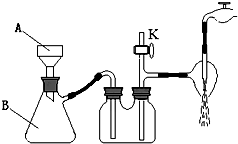 高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.
高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.| NaNO3 | KNO3 | NaCl | KCl | |
| 10°C | 80.5 | 20.9 | 35.7 | 31.0 |
| 100°C | 175 | 246 | 39.1 | 56.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
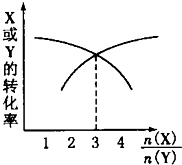 一定条件下,将X和Y两种气体按不同比例通入固定容积的密闭容器中,反应达平衡后,测得X、Y的转化率与起始时物质的量之比:
一定条件下,将X和Y两种气体按不同比例通入固定容积的密闭容器中,反应达平衡后,测得X、Y的转化率与起始时物质的量之比:| n(X) |
| n(Y) |
| 温度/℃ | 压强/kPa | Z的质量分数 |
| 200 | 101 | 0.40 |
| 300 | 101 | 0.48 |
| 400 | 202 | 0.52 |
| 400 | 303 | 0.52 |
| A、3X(g)+Y(g)?4Z(g);△H>0 |
| B、X(g)+3Y(g)?4Z(g);△H>0 |
| C、3X(g)+Y(g)?3Z(g);△H<0 |
| D、X(g)+3Y(g)?3Z(g);△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
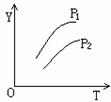
如下图所示,不同温度和压强下,在容积不变的密闭容器中对可逆反应:4L(g)![]() 2M(g)+N(g) △H>0平衡状态的影响(P1>P2),图中Y轴是指 ( )
2M(g)+N(g) △H>0平衡状态的影响(P1>P2),图中Y轴是指 ( )
A.气体混合物的平均相对分子质量
B.气体混合物的总物质的量浓度
C.L在气体混合物中的体积分数
D.气体混合物的密度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com