
【题目】航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉放热引发高氯酸铵分解。生成氮气、氯气、氧气还有水。完成下列填空:
(1)Al原子的最外层电子排布式为_____________,其电子云形状有____种。
(2)氯元素在元素周期表中的位置是_________,氮氧两元素非金属性强的是______。
(3)上述分解反应中的还原产物是________,1mol NH4ClO4分解时电子转移的物质的量为_________。
(4)NH4ClO4溶液中各离子浓度由大到小的排列顺序为___________。
(5)以AlCl3溶液为原料制取无水AlCl3,先制得AlCl3·6H2O晶体,主要操作包括____________,再在干燥的HCl气流中加热AlCl3·6H2O晶体,能进一步制取无水AlCl3,试结合化学方程式说明原因:_____。
【答案】3s23p1 2 第三周期第VIIA族 氧元素 氯气 7mol c(ClO4-)>c(NH4+)>c(H+)>c(OH-) 加热浓缩、冷却结晶 存在AlCl3+3H2O![]() Al(OH)3+3HCl,在干燥的HCl气流中,能抑制AlCl3的水解,且带走AlCl36H2O晶体受热产生的水蒸气,可得到纯净的AlCl3
Al(OH)3+3HCl,在干燥的HCl气流中,能抑制AlCl3的水解,且带走AlCl36H2O晶体受热产生的水蒸气,可得到纯净的AlCl3
【解析】
(1)Al在元素周期表中为13号元素,根据核外电子排布规律书写其最外层电子排布式;s能级电子云形状为球形,p能级电子云形状为哑铃形,据此作答;
(2)氯元素原子序数为17,结合元素周期表结构与元素周期律作答;
(3)高氯酸铵(NH4ClO4)分解生成氮气、氯气、氧气还有水,依据氧化还原反应规律作答;
(4)铵根离子会发生水解;
(5)铝离子水解生成盐酸易挥发,不能直接蒸发得到晶体,以此来解答。
(1)Al原子序数为13,依据电子排布规律可知,其最外层电子排布式为3s23p1,因s能级电子云形状为球形,p能级电子云形状为哑铃形,所以其电子云形状有2种,
故答案为:3s23p1;2;
(2)氯元素原子序数为17,在元素周期表中位于第三周期第VIIA族;同周期元素中,非金属性随着原子序数的递增而增大,所以氮氧两元素非金属性强的是氧,
故答案为:第三周期第VIIA族;氧元素;
(3)依据题意可知,高氯酸铵分解的化学方程式为:![]() ,氯元素从+7价降低到0价,被还原,得到的氯气为还原产物,其中1mol NH4ClO4分解时电子转移的物质的量为1×(7-0) = 7 mol,
,氯元素从+7价降低到0价,被还原,得到的氯气为还原产物,其中1mol NH4ClO4分解时电子转移的物质的量为1×(7-0) = 7 mol,
故答案为:氯气;7mol;
(4) NH4ClO4溶液中NH4+会发生水解生成一水合氨与H+,使溶液呈现酸性,所以其离子浓度大小顺序为:c(ClO4-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(ClO4-)>c(NH4+)>c(H+)>c(OH-);
(5)铝离子水解生成盐酸易挥发,不能直接蒸发得到晶体,则操作包括①加热浓缩,②冷却结晶;在第①步操作中应注意的事项是用玻璃棒不断搅拌溶液,当有晶体析出时停止加热.在干燥的HCl气流中加热AlCl36H2O晶体,能进一步制取无水AlCl3,其原因是存在AlCl3+3H2OAl(OH)3+3HCl,在干燥的HCl气流中,能抑制AlCl3的水解,且带走AlCl36H2O晶体受热产生的水蒸气,可得到纯净的AlCl3,
故答案为:加热浓缩、冷却结晶;存在AlCl3+3H2O![]() Al(OH)3+3HCl,在干燥的HCl气流中,能抑制AlCl3的水解,且带走AlCl36H2O晶体受热产生的水蒸气,可得到纯净的AlCl3。
Al(OH)3+3HCl,在干燥的HCl气流中,能抑制AlCl3的水解,且带走AlCl36H2O晶体受热产生的水蒸气,可得到纯净的AlCl3。


科目:高中化学 来源: 题型:
【题目】碳、氮、氧、磷、硫、铁,锌、铜等都是组成蛋白质的重要元素。回答下列问题:
(1)Fe的基态原子的核外电子排布式为_________,3d能级上的未成对电子数为____。
(2)在C、N、O、P、S五种元素中,第一电离能最大的元素是_____(填元素符号,下同),电负性最大的元素是______
(3)氨基乙酸(H2NCH2COOH)是蛋白质完全水解的产物之一,其中C原子的杂化轨道类型为______;1molH2NCH2COOH中含有![]() 键的数目为_____NA。
键的数目为_____NA。
(4)蛋白质在体内部分被氧化生成尿素[CO(NH2)2]、二氧化碳、水等排出体外。
①CO2、H2O分子的空间构型分别为_____、_____。
②尿素的熔点为132.7℃,其固体属于_____晶体。
③尿素易溶于水,其原因除都是极性分子外,还有_________。
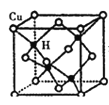
(5)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为____。若该晶体的密度为ρg·cm—3,阿伏加德罗常数的值为NA,则该晶胞的棱长为_____nm(用含ρ和NA的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】张青莲是我国著名的化学家,1991年他准确测得In的相对原子质量为114.818,被国际相对原子质量委员会采用为新的标准值。下列说法中,错误的是( )
A. ![]() In是In元素的一种核素 B.
In是In元素的一种核素 B. ![]() In原子核内有49个中子
In原子核内有49个中子
C. ![]() In原子核内质子数和中子数之和为115 D.
In原子核内质子数和中子数之和为115 D. ![]() In原子核外有49个电子
In原子核外有49个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对FeCl3分别与Na2SO3、NaHSO3的反应进行探究。
(甲同学的实验)
装置 | 编号 | 试剂X | 实验现象 |
| I | Na2SO3溶液(pH≈9) | 闭合开关后灵敏电流计指针发生偏转 |
II | NaHSO3溶液(pH≈5) | 闭合开关后灵敏电流计指针未发生偏转 |
(1)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。结合化学用语说明浓盐酸的作用:。
(2)甲同学探究实验I的电极产物______________。
①取少量Na2SO3溶液电极附近的混合液,加入______________,产生白色沉淀,证明产生了![]() 。
。
②该同学又设计实验探究另一电极的产物,其实验方案为______________。
(3)实验I中负极的电极反应式为______________。
(乙同学的实验)
乙同学进一步探究FeCl3溶液与NaHSO3溶液能否发生反应,设计、完成实验并记录如下:
装置 | 编号 | 反应时间 | 实验现象 |
| III | 0~1 min | 产生红色沉淀,有刺激性气味气体逸出 |
1~30 min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 | ||
30 min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
(4)乙同学认为刺激性气味气体的产生原因有两种可能,用离子方程式表示②的可能原因。
① Fe3++3![]()
![]() Fe(OH)3 +3SO2;②______________。
Fe(OH)3 +3SO2;②______________。
(5)查阅资料:溶液中Fe3+、![]() 、OH-三种微粒会形成红色配合物并存在如下转化:
、OH-三种微粒会形成红色配合物并存在如下转化:
![]()
从反应速率和化学平衡两个角度解释1~30 min的实验现象:______________。
(6)解释30 min后上层溶液又变为浅红色的可能原因:______________。
(实验反思)
(7)分别对比I和II、II和III,FeCl3能否与Na2SO3或NaHSO3发生氧化还原反应和有关(写出两条)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4 molA和2molB进行如下反应:
3A(g)+2B(g)![]() 4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
A. 前2min,D的平均反应速率为0.2mol/(L·min)
B. 此时,B的平衡转化率是40%
C. 增加B,平衡向右移动,B的平衡转化率增大
D. 增大该体系的压强,平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车废气排放已成为城市大气污染的重要来源,汽车排气系统中安装三元催化器可同时将废气中的三种主要有害物质转化为无害物质。
反应Ⅰ:4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) ΔH=-1196 kJ/mol
N2(g)+4CO2(g) ΔH=-1196 kJ/mol
反应Ⅱ:2CO(g)+2NO(g) ![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
(1)已知: ①N2(g) + O2(g)=2NO(g) ΔH=+180.5kJ/mol
② 2CO(g) + O2(g)=2CO2(g) ΔH=-566.0kJ/mol
则反应Ⅱ的 ΔH=_________,ΔS______0(填“>”、“<”或“=”)
(2)进一步探究上述反应Ⅱ中 NO 的平衡转化率与压强、温度的关系,得到图 1 所示的曲线。根据图像,控制反应 II进行的合适条件:温度为_________________,压强为常压(1.01MPa) ,选择该压强的原因是________________________。

(3)模拟反应Ⅰ:将一定量的 CO 与 NO2 充入装有催化剂的注射器中进行反应。图2是在拉伸或压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小) 根据图像,回答下列问题:
①a、 c、 e 三点 c(NO2)由小到大的顺序是____________________;
②e 点速率:υ(正)_________υ(逆)(填“>”、“<”或“=”,下同);
③若注射器绝热,平衡常数 K(b)_________ K(d)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A. 标准状况下,铁在22.4L氯气中完全燃烧时转移电子数为3NA
B. 1 L 0.1 mol·L1的NaHCO3溶液中![]() 和
和![]() 离子数之和为0.1NA
离子数之和为0.1NA
C. 在一定温度下64gSO2与足量氧气充分反应,转移电子数为4NA
D. 含有NA个Fe( OH)3胶粒的氢氧化铁胶体中,铁元素的质量大于56g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池的工作原理:Zn+2MnO2+2H2O![]() 2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1x)Fe2O4,其工艺流程如图所示:
2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1x)Fe2O4,其工艺流程如图所示:

(1)已知MnxZn(1x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为___________。
(2)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:_________________________________。
(3)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:______________________、_______。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L1,c(Fe2+)+c(Fe3+)=b mol·L1,滤液体积为1 m3,“调铁”工序中,需加入的铁粉质量为___________kg(忽略溶液体积变化,用含a、b的代数式表示)。
(4)在“氧化”工序中,加入双氧水的目的是把 Fe 2+ 氧化为 Fe 3+;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是______________________。
(5)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐中除含有NaCl外,还含有![]() 以及泥沙等杂质。制备精盐的各步操作流程如下:
以及泥沙等杂质。制备精盐的各步操作流程如下:

(1)在第⑦步蒸发过程中要用玻璃棒搅拌,目的是__________。
(2)第②、④步操作的目的分别是除去粗盐中的![]() 和
和![]() ,需要加入的试剂依次是________(填化学式)。
,需要加入的试剂依次是________(填化学式)。
(3)第⑥步操作中发生反应的化学方程式为________。
(4)在第③步操作中,选择的除杂试剂不能是KOH溶液,理由是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com