
【化学——选修5:有机化学基础】(15分)
白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。DBP是塑化剂的一种,可由下列路线合成:
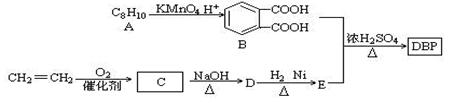
已知以下信息:
①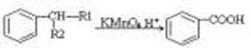
②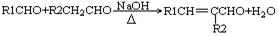
(-R1、-R2表示氢原子或烃基)
(1)A的结构简式 ,D的结构简式是 ,
D→E的反应类型 。
(2)D和H2 1︰1反应生成E,则E官能团名称为_________,DBP的分子式为 .(3)由B和E以物质的量比1︰2合成DBP的化学方程式: 。
(4)写出同时符合下列条件的B的所有同分异构体结构简式 。
①能和NaHCO3溶液反应生成CO2 ③能使FeC13溶液发生显色反应
②能发生银镜反应 ④苯环上含碳基团处于对位
(5)写出B与碳酸氢钠溶液反应的方程式 。
写出C生成D的反应的方程式 。
【知识点】有机合成、有机反应、反应类型、官能团、同分异构体
【答案解析】(1)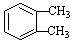 CH3CH=CHCHO 加成(还原)反应 (每空1分)
CH3CH=CHCHO 加成(还原)反应 (每空1分)
(2)碳碳双键 羟基 C16H18O4
(3)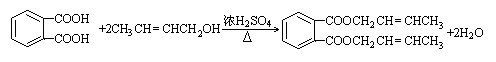
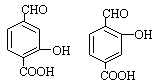
(4)
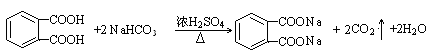
(5)
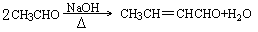
解析:(1)通过B和已知1可推断A为: ,C为乙醛,通过已知2的反应可知D为CH3CH=CHCHO
,C为乙醛,通过已知2的反应可知D为CH3CH=CHCHO
(2)D和H2 1︰1反应生成E,又因为E和B是酯化反应,所以D中的醛基被还原(加成)成羟基,所以E中官能团为碳碳双键和羟基 。有第3问可知DBP的分子式C16H18O4
(3) 由B和E以物质的量比1︰2合成DBP的化学方程式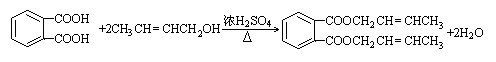
(4) B的所有同分异构体结构简式;能和NaHCO3溶液反应生成CO2羧基,能发生银镜反应说明含有醛基,能使FeC13溶液发生显色反应说明含有酚羟基,苯环上含碳基团处于对位,综合上诉为
(5)羧基和碳酸氢钠溶液制碳酸,利用的是羧基的酸性大于碳酸的酸性。

根据已知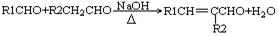
当-R1为甲基、-R2表示氢原子可得 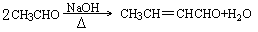
【思路点拨】本题考查有机化学基本反应类型,官能团具有的特定性质:酯的水解、醇、醛的氧化,其中同分异构体的书写是难点,注意结构的对称性,考查学生的逻辑思维能力。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式的是( )
A.碳酸钠溶于足量盐酸中 Na2CO3+2H+=2Na++CO2?+H2O
B.氧化钠与稀硫酸的反应 Na2O+2H+ = 2Na++H2O
C.氢氧化钡溶液与硫酸铜溶液反应 Ba2+ + SO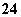 = BaSO4↓
= BaSO4↓
D.铁片插入稀硫酸溶液中 Fe + 2H+ = Fe3+ + H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀盐酸,沉淀不溶解,则该溶液中
A. 一定有SO42- B. 可能有SO42- 或Ag+
C. 一定无Ag+ D. 还可能有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活是紧密相联的,下列关于生活与化学的说法不正确的是
A.从海水提取物质不一定都必须通过化学反应才能实现
B.大量的氮、磷废水排入海洋,易引发赤潮
C.为了防止中秋月饼等富脂食品氧化变质,延长食品保质期,在包装袋中常放入生石灰
D.保护加酶洗衣粉的洗涤效果,应用温水溶解洗衣粉
查看答案和解析>>
科目:高中化学 来源: 题型:
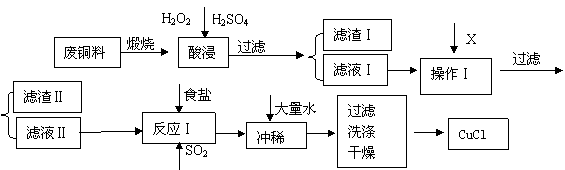
CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.8 | 4.7 |
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是: 。
(2)操作Ⅰ为调节溶液的PH值,范围为 ,加入的物质X可以是( )
A、CuO B、Cu(OH)2 C、NaOH 溶液 D、CaCO3
(3)滤渣Ⅱ的主要成分是 。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式:
。
(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是: 。
(6)常温下,已知CuOH的KSP为1.0×10-14,则Cu++H2O  CuOH + H+的平衡常数为: 。
CuOH + H+的平衡常数为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是
A.原子核外每一能层最多可容纳的电子数2n2(n为能层序数)
B.能层序数越大,s原子轨道的半径越大
C.各能级包含的原子轨道数按s、p、d、f的顺序依次为1、3、5、7
D.1个原子轨道里最多只能容纳2个电子,且自旋方向相同
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素甲和乙,甲原子的最外层电子数为a,次外层电子数为b;乙原子的M层电子数为(a – b – 1),L层电子数为(a + b)。 则甲、乙两元素形成的化合物具有的性质是
则甲、乙两元素形成的化合物具有的性质是
①与水反应 ②与硫酸反应 ③与氢氧化钠溶液反应 ④与氯气反应
A.①② B.②③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知 X、Y、Z、Q、R、E六种元素中,原子序数的大小关系为X<Y<Z<Q<R<E,其结构
或性质信息如下表。
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数。 |
| Y | 原子核外的L层有3个未成对电子。 |
| Z | 在元素周期表的各元素中电负性仅小于氟。 |
| Q | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | 原子序数比R大3 |
请根据信息回答有关问题:
(1)元素Y的原子核外共有 种不同运动状态的电子,有 种不同能级的电子。
(2)X、Y、Z三种元素的电负性由高到低的排列次序依次为(写元素符号) 。
(3)R的最高化合价为 ;R的一种配合物的化学式为RCl3·6H2O。已知0.01 molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(4) 元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心离子为(写化学式) ,
配位体为(写化学式) ,x 的值为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作合理的是( )
A.用稀硫酸清洗做焰色反应的铂丝
B.用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液
C.用100mL容量瓶配制50mL 0.1 mol·L-1的盐酸
D.测NaOH熔点时可以将NaOH放入石英坩埚中高温熔化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com