
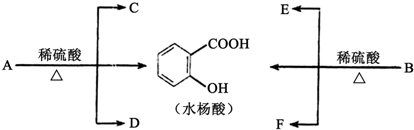
| 2n |
| 5 |
| 2n |
| 5 |
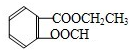 ,B为
,B为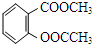 ,据此解答.
,据此解答.| 2n |
| 5 |
| 2n |
| 5 |
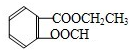 ,B为
,B为 ,
, ,故答案为:
,故答案为: ;
; 、
、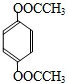 、
、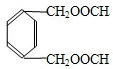 ,故答案为:3;
,故答案为:3; ,此反应的化学方程式为:
,此反应的化学方程式为: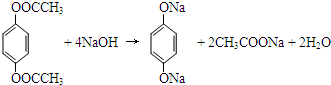 ,
, .
.


 特高级教师点拨系列答案
特高级教师点拨系列答案 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将22.4 L HCl气体溶于水稀释至200 mL |
| B、将36.5 g HCl气体溶于200 mL水中 |
| C、取10 mol/L的盐酸100 mL加水100 mL |
| D、取10 mol/L的盐酸100 mL加水稀释至200 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
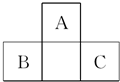 如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答:
如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、n(Ca2+)增大 |
| B、c(Ca2+)减小 |
| C、pH增大 |
| D、c(OH-)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3++3H2O═Fe(OH)3+3H+ |
| B、HSO3-+H2O?H2SO3+OH- |
| C、CH3COO-+H2O?CH3COOH+OH- |
| D、A13++3HCO3-═Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com